Häufig gestellte Fragen (FAQ)
Vitamine und Spurenelemente
Wir verwenden diese stabilisierenden Spezialröhrchen auch, allerdings nur in Berlin bzw. wenn das Blut am selben Tag im Labor eingeht. Bei allen Proben, die wir overnight aus dem Bundesgebiet bekommen, würden auch diese Stabilisierungsröhrchen nicht helfen, da es nach 6-8 h Lagerungszeit auch mit dem Stabilisator zu einem Anstieg von Homocystein in der Blutprobe und damit zu falsch erhöhten Werten kommt.
Warum? Homocystein ist ein Zwischenprodukt im Methionin-Stoffwechsel, der in allen Körperzellen, auch in Blutzellen abläuft. Nach der Blutentnahme läuft der Stoffwechsel weiter, d.h. die Blutzellen produzieren weiter Homocystein und geben es nach außen ab, wodurch die Konzentration im Serum künstlich ansteigt.
Das Homocystein-Spezialröhrchen enthält saures Citrat, einen Enzymhemmer, welcher den Methionin-Stoffwechsel und damit den Anstieg von Homocystein für 6-8 h verzögert. Bei längerer Lagerung macht es dagegen keinen Unterschied, ob diese Enzymhemmung stattfindet oder nicht. Nach 24 h würde es daher auch mit den Spezialröhrchen zu einem falsch erhöhten Homocystein-Wert kommen. Daher ist es, egal ob man Serum- oder Homocystein-Röhrchen verwendet, bei Blutlagerung über 8 h nötig, durch Zentrifugation das Serum von den Blutzellen zu trennen. Da auch das Gel in den üblichen Serumröhrchen für die kleine schwefelhaltige Aminosäure Homocystein durchlässig ist, muss das Serum zudem in ein Neutralröhrchen überführt werden. Das alles ist aufwändig, aber nur so sind verlässliche Homocystein-Werte möglich.
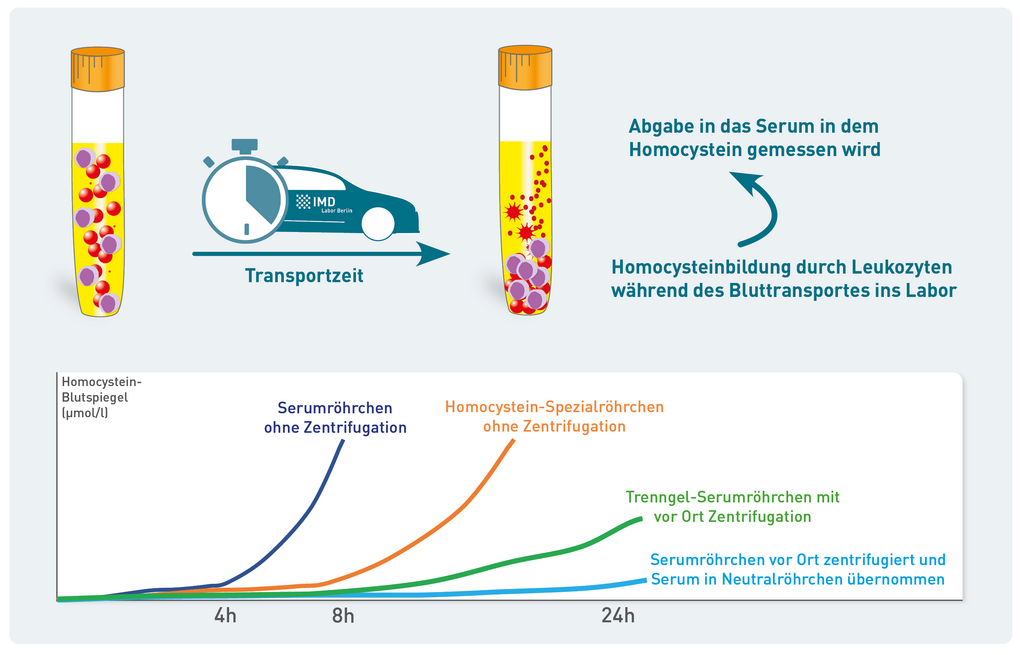
Nein, das ist nicht möglich. Die Äquivalenztabelle auf der Rückseite unserer Diagnostik-Information (Link zum PDF) gibt korrelierende Mittelwerte des freien Vitamin D und des Gesamt-25-[OH]-Vitamin D in der Referenzpopulation an. Einzelne Patienten weichen von diesen Durchschnittswerten deutlich ab, denn der Anteil des freien Vitamin D wird von individuellen Faktoren erheblich beeinflusst. Zu den individuell sehr variablen Einflussgrößen zählen z.B. die Leber- und Nierenfunktion, der Hormonstatus sowie genetische Varianten. Die Äquivalenztabelle bildet diese biologische Varianz nicht ab. Ihre Bedeutung liegt vielmehr darin, in der klinischen Praxis verankerte Zielwerte des Gesamt-25-[OH]-Vitamin D zumindest näherungsweise, auf das freie Vitamin D übertragen zu können. Für eine aussagekräftige Bewertung und klinisch relevante Beurteilung eines einzelnen Patienten ist die Tabelle jedoch ungeeignet – hier ist die direkte Messung des freien Vitamin D die empfohlene und einzig valide Option.
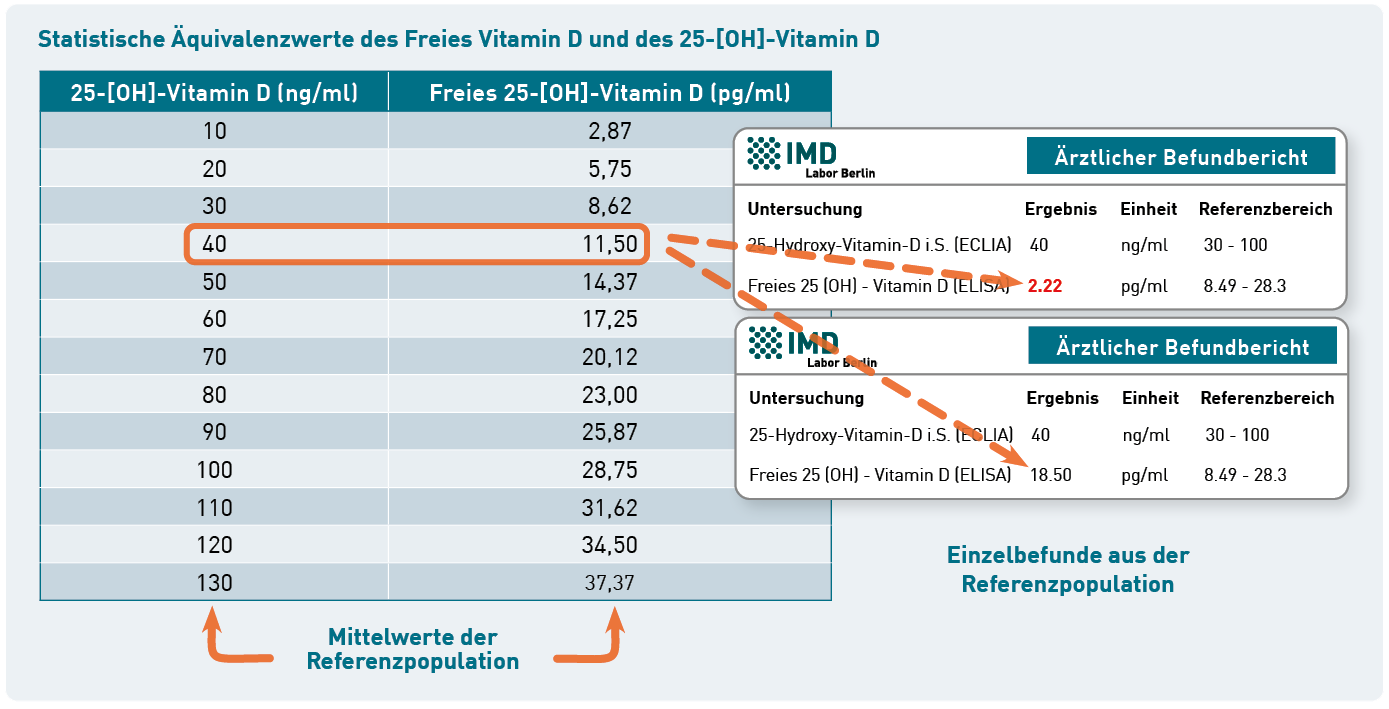
Untercarboxyliertes Osteocalcin (ucOC) wird von Osteoblasten produziert und spielt eine wichtige Rolle im Knochenstoffwechsel. Um seine volle Funktion im Knochen zu erfüllen, muss ucOC carboxyliert werden. Dieser Schritt benötigt Vitamin K als Cofaktor. Ein Mangel an Vitamin K führt daher zu einer verminderten Carboxylierung und ucOC steigt an. Zeigt der Laborbefund ein erhöhtes ucOC, obwohl der Patient ausreichend Vitamin K zuführt oder sogar supplementiert, stellt sich die Frage, welche weiteren Ursachen einen funktionellen Mangel und einen erhöhten ucOC-Wert bedingen können. Hierzu zählen:
- Malabsorption: Bedingungen, die die Aufnahme von Nährstoffen im Darm beeinträchtigen (z. B. Zöliakie, Morbus Crohn oder chronische Pankreatitis).
- Geringe Produktion im Mikrobiom: Der Anteil des von Darmbakterien produzierten Vitamin K2 am Gesamt-Versorgungsstatus wird in der Forschung diskutiert.
- Lebererkrankungen: Die Leber spielt eine zentrale Rolle im Vitamin-K-Stoffwechsel (Speicherfunktion, Konvertierung in aktive Form). Erkrankungen der Leber können somit die Fähigkeit des Körpers zur Nutzung von Vitamin K beeinträchtigen.
- Nierenerkrankungen: Chronische Nierenerkrankungen können den Stoffwechsel von Vitamin K beeinträchtigen (Aufnahme und Reabsorption).
- Medikamenteneinnahme: Bestimmte Medikamente, wie Vitamin-K-Antagonisten (z. B. Warfarin), die zur Blutgerinnungshemmung eingesetzt werden, hemmen die Wirkung von Vitamin K.
- Alter: Mit zunehmendem Alter kann die Effizienz der Vitamin-K-Wiederverwertung und die Fähigkeit zur Carboxylierung von Osteocalcin abnehmen.
- Genetische Faktoren: Bestimmte genetische Varianten (z. B. VKORC1-Gen für Recycling-Prozesse, GGCX-Gen für Carboxylierungsschritt) können die Carboxylierungseffizienz von Osteocalcin beeinflussen.
Unabhängig vom Vitamin-K-Status ist die Aussagekraft des Biomarkers ucOC bei Veränderungen des Knochenstoffwechsels eingeschränkt. Insbesondere in Phasen des Knochenwachstums (z. B. bei Kindern oder bei Frakturen) sowie bei osteoporotischen Veränderungen der Osteoblastenaktivität gibt ucOC die Vitamin-K-Versorgung unzureichend wieder. Wir empfehlen in diesen Fällen stattdessen die direkte Bestimmung von Vitamin K1, sowie der Vitamin-K2-Metabolite MK-4 und MK-7 im Serum.
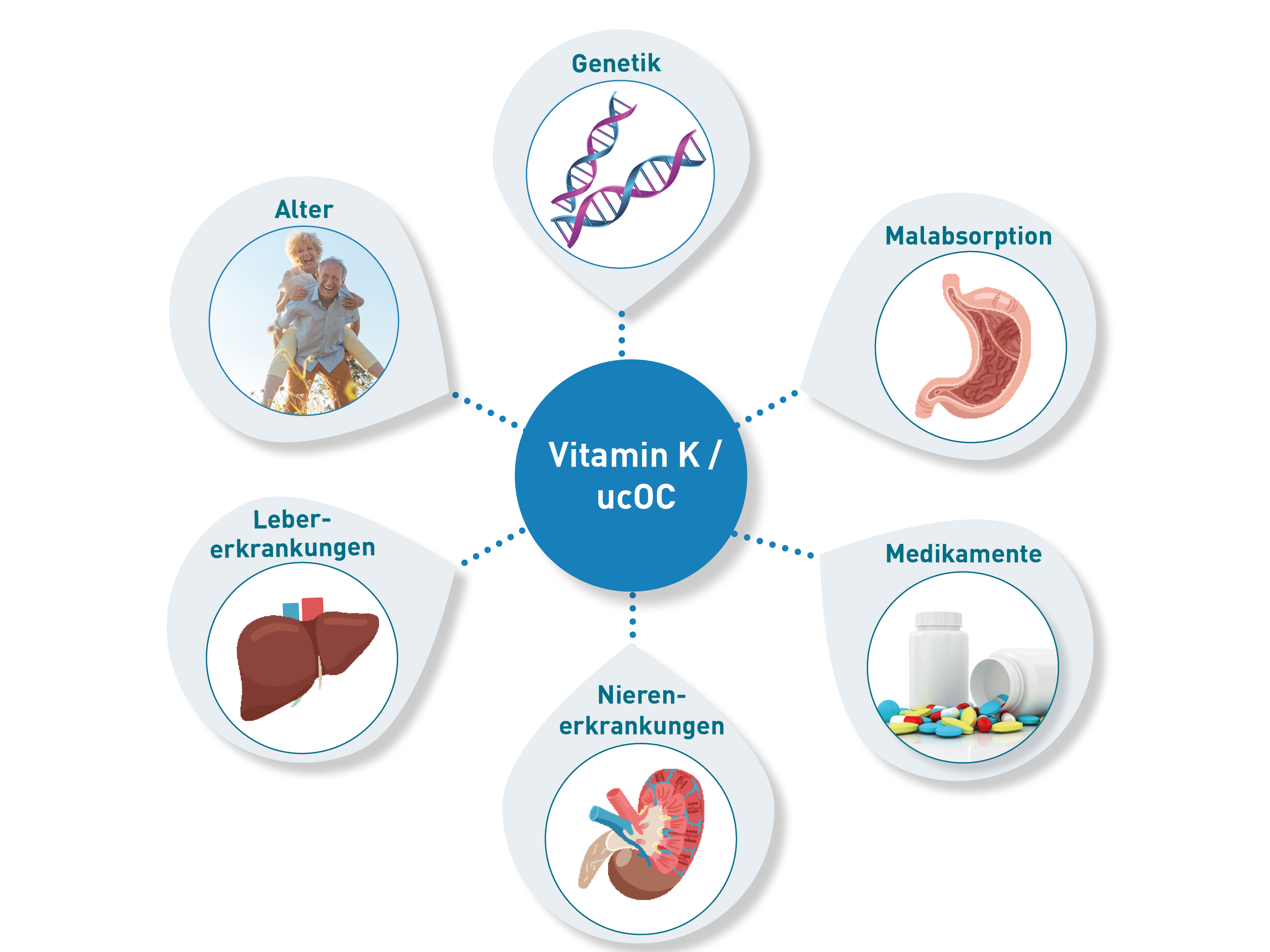
Ja – aber nur dann, wenn in den zu vergleichenden Laboren dasselbe Spektrum an Fettsäuren gemessen wird. Der Omega 3-Index berechnet sich nämlich nicht allein aus EPA und DHA, sondern als prozentualer Anteil dieser beiden Fettsäuren an allen langkettigen Fettsäuren. Vergleichbar sind die Ergebnisse des Omega 3-Index also immer dann, wenn tatsächlich das gleiche Set der langkettigen Fettsäuren gemessen wird, also die Bezugsgröße 100% identisch ist. Das am IMD gemessene Spektrum entspricht exakt den Fettsäuren, die im Rahmen der Studien zum Omega 3-Index gemessen wurden (u. a. von Schacky und Harris, 2007). Sogar bei dem kleinen Profil „Omega 3-Index“ werden für die Berechnung im Hintergrund alle diese Fettsäuren analysiert, auch wenn auf dem Laborbefund nur EPA und DHA übermittelt werden. Das zweite wichtige Kriterium für die Vergleichbarkeit ist das Untersuchungsmaterial: Der Omega 3-Index muss aus EDTA-Blut gemessen werden, weil nur die Fettsäuren der Erythrozytenmembranen Aussagen über den langfristigen Versorgungsstatus erlauben. Plasma, Serum oder Vollblut sind nicht vergleichbar. Am IMD erfolgt die Analyse der langkettigen Fettsäuren ausschließlich aus venös entnommenem EDTA-Blut. Auf der Grundlage dieser entscheidenden Merkmale – dem Fettsäurespektrum und der Analyse dieser Fettsäuren in der Erythrozytenmembran – ist der, am IMD Berlin ermittelte, Omega 3-Index mit Befunden aus Laboren vergleichbar, die nach denselben Kriterien arbeiten.
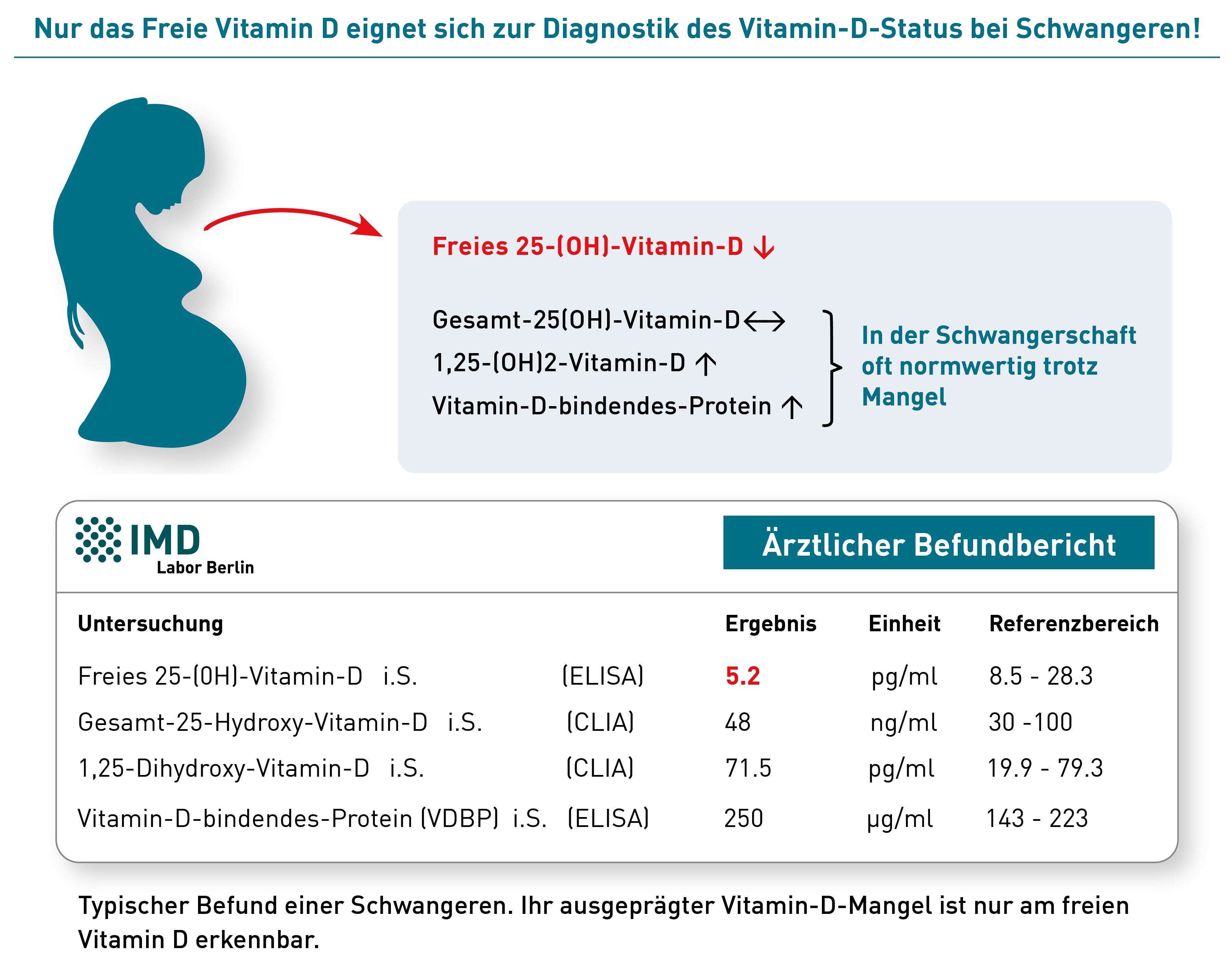
Während der Schwangerschaft ist der Vitamin-D-Status von besonderer Bedeutung für die Gesundheit von Mutter und Kind. Unzureichende Versorgung ist ein Risikofaktor für Schwangerschaftshypertonie und -diabetes sowie für Frühgeburt, Wachstumsstörungen, niedriges Geburtsgewicht, erhöhte perinatale Mortalität und Morbidität (z. B. schlechtem APGAR-Score) und für die Entwicklung des metabolischen Syndroms im Erwachsenenalter.
Das erforderliche Monitoring des Vitamin-D-Status erfolgt idealerweise durch Messung von freiem 25(OH)-Vitamin-D und 1,25-(OH)2-Vitamin-D vor geplanter Schwangerschaft, in der Frühschwangerschaft und im letzten Trimenon. Wichtig ist die Messung von freiem Vitamin D, da es das biologisch aktive 25(OH)-Vitamin-D widerspiegelt und dieser Messwert – anders als das Gesamt-25(OH)-Vitamin-D – in der Schwangerschaft nicht Östradiol-bedingt fälschlich eine gute Versorgung vortäuscht. Östradiol, das in der Schwangerschaft deutlich ansteigt, ist einer der stärksten Stimuli für die Synthese von Vitamin D Bindungsprotein (VDBP) in der Leber. Die VDBP-Serumkonzentration wiederum beeinflusst die Menge an Gesamt-(OH)-Vitamin-D im Blut. Gesamt-25(OH)-Vitamin-D kann daher in der Schwangerschaft Östradiol-bedingt konstant auf einem guten Niveau bleiben, auch wenn das bioverfügbare freie 25(OH)-Vitamin-D deutlich zurückgeht und eine Mangelsituation entsteht. Dieser Zusammenhang zeigt den besonderen Wert des Östradiol-unabhängigen, freien 25(OH)-Vitamin-D in der Schwangerschaft.
Eine weitere wenig beachtete Besonderheit in der Schwangerschaft ist der Anstieg von 1,25-(OH)2-Vitamin-D. Er ist auf die plazentale Expression der 1-alpha-Hydroxylase zurückzuführen, ein Enzym, das die in höheren Konzentrationen sonst nur in der Niere vorkommt. Dies hat zur Folge, dass die 1,25-(OH)2-Vitamin-D-Spiegel bei Schwangeren etwa doppelt so hoch sind wie bei Frauen, die nicht schwanger sind. In anderen Worten: Für die Allgemeinbevölkerung normwertige Vitamin-D-Parameter können bei Schwangeren mit einer Vitamin-D-Unterversorgung verbunden sein. Nur freies Vitamin D beschreibt auch bei Schwangeren zuverlässig den Vitamin D Status.
Bei Untersuchungen des Vitamin-B12-Status kommt es vor, dass der Laborbefund einen deutlich erhöhten Wert zeigt, der sich nicht durch eine Substitution erklären lässt. In diesem Fällen sollten folgende Erklärungsmöglichkeiten beachtet werden:
• Der Test könnte zeitlich zu nah nach der Einnahme von Vitamin-B12-Präparaten durchgeführt worden sein. Empfohlen sind 7-10 Tage Karenzzeit zwischen Substitution (Injektion oder oral) und der Blutentnahme.
• Die Vitamin-B12-Konzentrationsmessung könnte durch IgG-IgM-Vitamin-B12-Immunkomplexe sowie Autoantikörper gegen den Intrinsic-Faktor gestört worden sein. Dies kann vermieden werden, wenn der bioaktive Vitamin-B12-Assay verwendet wird, da er von diesen Faktoren nicht beeinflusst wird.
• Es liegt eine Erkrankung vor, die die Produktion von Haptocorrinen /Transcobalaminen steigert, z.B.:
- Lebererkrankungen (Hepatitis, Leberzirrhose, alkoholische Leber)
- Tumorerkrankungen (Leber, Brust, Darm, Magen, Bauchspeicheldrüse)
- Blutkrankheiten (CML, Polycythaemia vera, Myelofibrose, Hypereosinophiles Syndrom, akute Leukämie)
• In geringerem Ausmaß führt auch eine Retention der Transportproteine, z.B. bei Nierenerkrankungen, zu erhöhten B12-Werten.
• Es liegt eine Verwertungsstörung vor, d.h. es ist nicht genügend Transcobalamin II-gebundenes Vitamin B12 (HoloTC) verfügbar. Hier empfiehlt sich die Messung des HoloTC.
• Bei Darmerkrankungen kann es ebenfalls durch bakterielle Überwucherung im Darm zu erhöhter Produktion von Vitamin-B12-Analoga durch Bakterien kommen.
Wir empfehlen folgendes Vorgehen:
- Messung kontrollieren, ggf. unter Beachtung der Karenzzeit und über das bioaktive Vitamin B12, wie oben beschrieben.
- Physiologische Vitamin-B12-Schwankungen sind wahrscheinlich ohne klinische Relevanz.
- Persistierende Vitamin-B12-Erhöhungen sind abzuklären, da sie auf schwerwiegende Erkrankungen hinweisen können (siehe oben).

Ja, bei Überwachung des Vitamin D-Stoffwechsels in der Schwangerschaft sind mehrere Besonderheiten zu beachten:
- Die Konzentration von totalem 25OH-Vitamin D steigt im Verlauf der Schwangerschaft deutlich an, weil Östrogene die Synthese von „Vitamin D Bindendem Protein“ (VDBP) stimulieren. Dieser Anstieg von VDBP führt jedoch nicht zu einem Anstieg des biologisch aktiven, freien Vitamin D. Das herkömmliche 25OH-Vitamin D ist daher bei Schwangeren schwierig zu interpretieren und die direkte Messung des freien Vitamin D umso bedeutsamer.
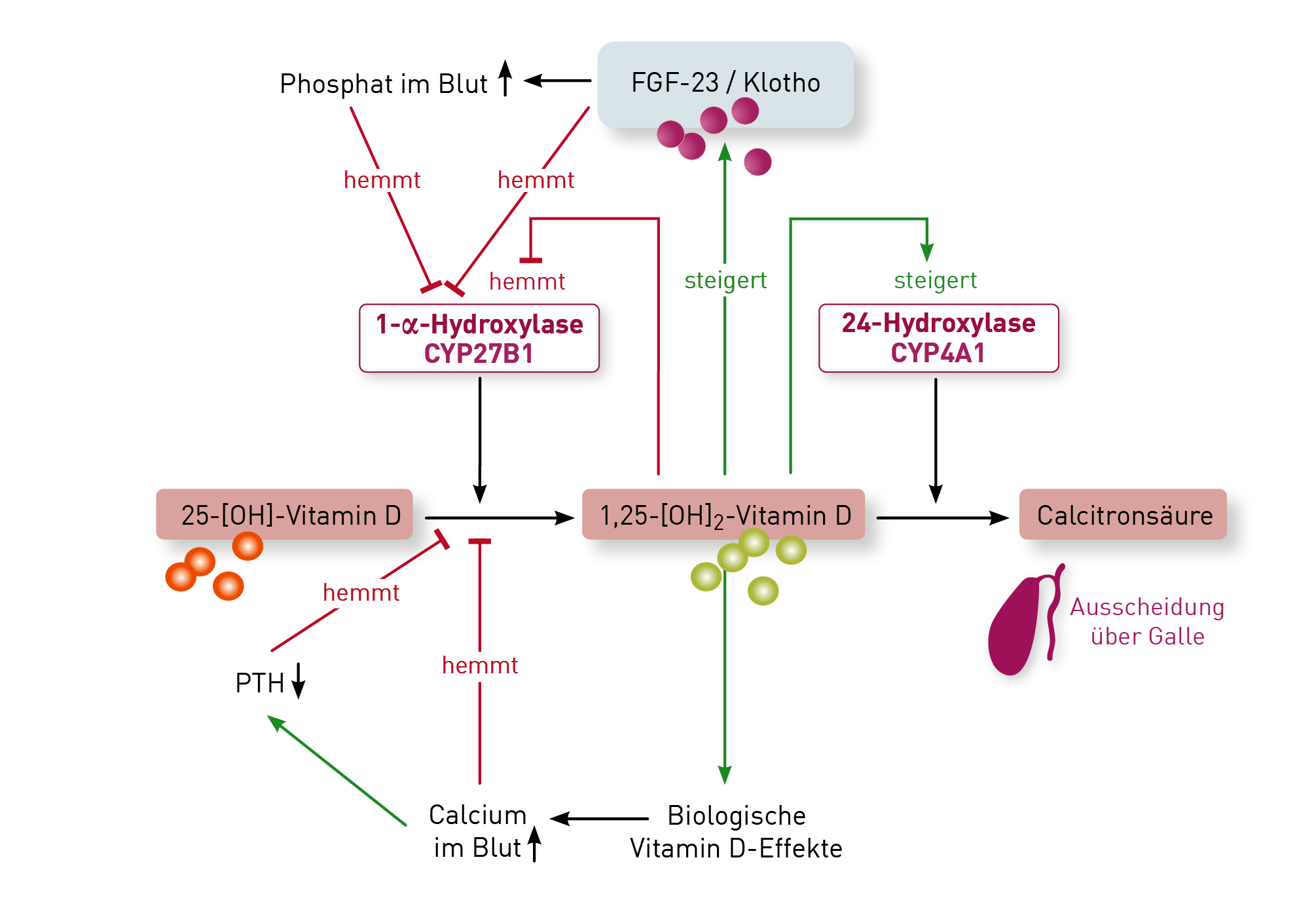
- Die Plazenta enthält hohe Konzentrationen des Enzyms 1-alpha-Hydroxylase und produziert daher große Mengen an 1,25 (OH)2-Vitamin D (siehe Abbildung). Eine gesunde Schwangere muss entsprechend etwa doppelt so hohe 1,25 (OH)2-Vitamin D-Konzentrationen aufweisen – scheinbar normale (d.h. für nicht-schwangere Frauen normwertige) 1,25 (OH)2-Vitamin D- Konzentrationen deuten bei Schwangeren auf erhebliche Probleme in der Plazenta hin.
- Sehr seltene, mütterliche und kindliche Gen-Defekte, z.B. im Gen der 24-Hydroxylase (siehe Abbildung), können zu bedrohlichen Hyperkalzämien des Neugeborenen führen, insbesondere wenn die Mutter während der Schwangerschaft mit hohen Dosen Vitamin D substituiert wurde. Freies 25(OH)-Vitamin D und 1,25 (OH)2-Vitamin D sollten daher im ersten und dritten Trimenon überprüft und als Richtwert für einen möglichen Substitutionsbedarf herangezogen werden. Bei Verdacht auf dieses Krankheitsbild ist auch eine Bestimmung von PTH und die entsprechende Gendiagnostik hilfreich (PTH ist bei diesem Gendefekt regelhaft supprimiert).
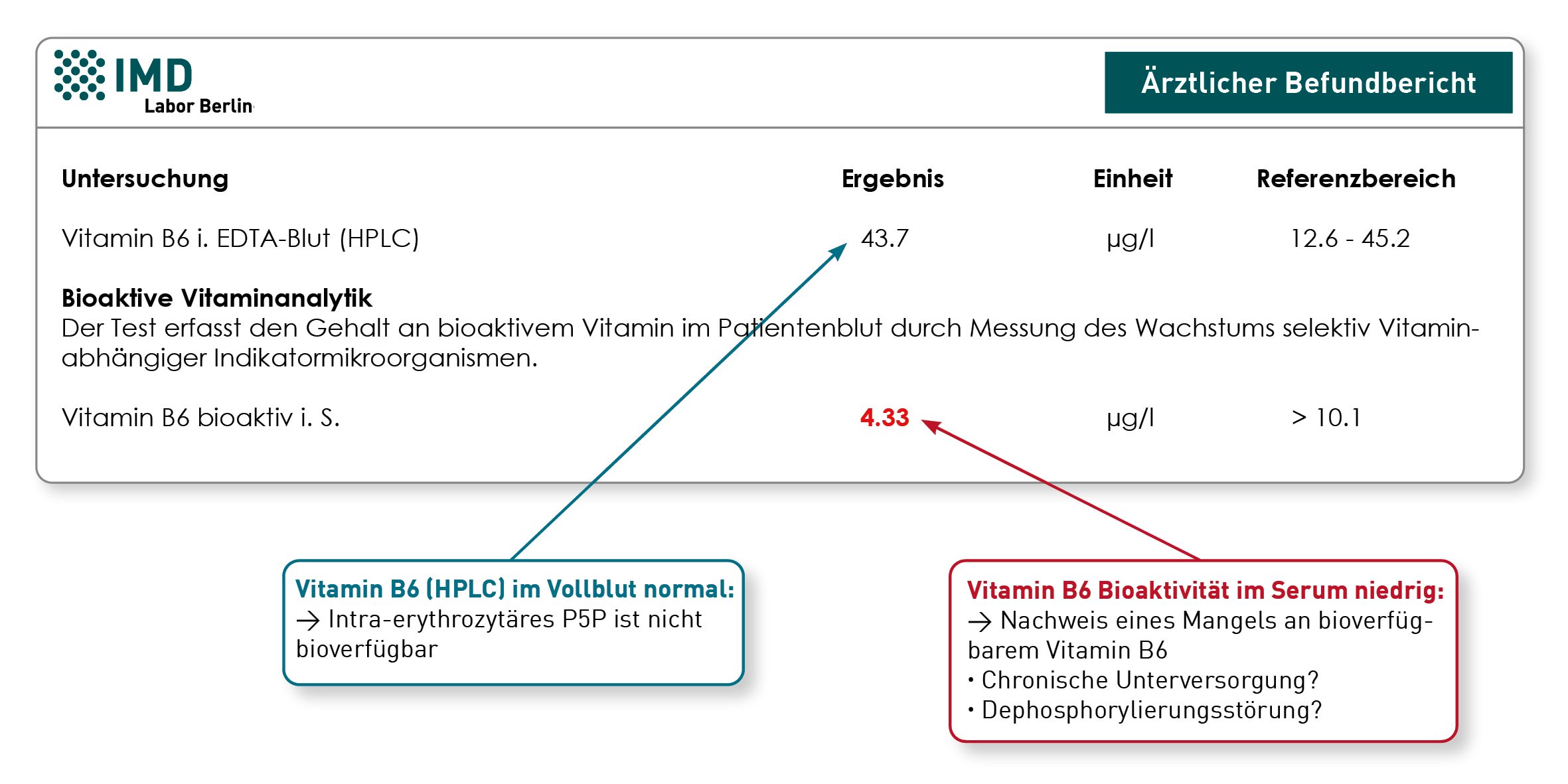
Das zur oralen Vitamin B6-Substitution häufig verwendete Pyridoxin wird in den roten Blutkörperchen rasch in Pyridoxalphosphat (P5P) umgewandelt. Am höchsten ist die intra-erythrozytäre P5P-Konzentration 1-2 Stunden nach der oralen Einnahme. Anschließend wird P5P zu Pyridoxal metabolisiert und in dieser Form wieder ans Plasma abgegeben und über das Blut verteilt. Pyridoxal kann direkt ins Gewebe aufgenommen werden. Aufgrund dieser Verstoffwechslung lassen sich zwei Erklärungen für die scheinbar diskrepanten Vitamin B6-Ergebnisse ableiten:
1) Der Patient hat kurz vor der Blutentnahme ein Substitutionspräparat eingenommen. Das aufgenommene Vitamin B6 liegt nun in hohen Konzentrationen in den Erythrozyten in Form des P5P vor, welches durch die Vollblut-Bestimmung in der HPLC erfasst wird. Liegt generell ein Mangelzustand vor, wird das ins Plasma abgegebene Pyridoxal relativ schnell ins Gewebe aufgenommen. Das folglich niedrige bioaktive Vitamin B6 spiegelt die chronische Mangelsituation wieder. Dies zeigt, dass anders als bei vielen anderen Mikronährstoffen bei Vitamin B6 gerade nicht die Vollblutanalyse, sondern die Serumanalyse den langfristigen Versorgungsstatus abbildet.
2) Kann Punkt 1 ausgeschlossen werden, könnte eine Dephosphorylierungsstörung vorliegen, wodurch die Umwandlung/Dephosphorylierung von P5P gehemmt ist. Da nur die dephosphorylierte Form aus den Erythrozyten ins Plasma abgegeben wird, akkumulieren hohe P5P-Spiegel in den roten Blutkörperchen, ohne dass das Gewebe mit Vitamin B6 versorgt wird. Hohes P5P im Vollblut wäre in diesem Fall Ausdruck eines funktionellen Mangels.
In der Praxis beobachten Therapeuten immer wieder, dass Patienten mit normalem/erhöhtem HPLC-Vitamin B6 im Vollblut und niedrigem bioaktiven Vitamin B6 im Serum von einer Vitamin B6-Gabe profitieren. Ein Monitoring ist hier nur über die Bioaktivität messbar.
Da überschüssiges Vitamin C effizient ausgeschieden wird, spielt die Labordiagnostik bei Verdacht auf Vitamin C-Mangel eine untergeordnete Rolle. Vitamin C kann im Gegensatz zu anderen Mikronährstoffen durchaus „blind“ supplementiert werden. Wichtig ist allerdings vor Hochdosistherapie der Ausschluss einer genetischen Glukose-6-Phosphat-Dehydrogenase (G6PD)-Defizienz. Diese kann im Labor über den einfachen G6PD-Aktivitätstest detektiert werden.
Soll Vitamin C im Einzelfall dennoch gemessen werden, ist die anfällige Präanalytik zu beachten. Vitamin C ist lichtempfindlich und wird noch nach der Blutentnahme von den Zellen in der Blutprobe verbraucht. Dies kann zu falsch niedrigen Konzentrationen führen. Aufgrund dieser präanalytischen Anfälligkeit empfehlen wir eine Blutentnahme im Labor vor Ort.
Alternativ zur direkten Bestimmung kann das „Aminosäureprofil Stoffwechsel“ einen Hinweis auf die Vitamin C-Versorgung geben. Ohne Vitamin C kann die Aminosäure Prolin nicht in Hydroxyprolin umgewandelt werden. Niedriges Hydroxyprolin bei normalem bis hohem Prolin weist auf eine unzureichende Vitamin C-Zufuhr hin. Das Verhältnis von Hydroxyprolin zu Prolin kann daher bei guter Verfügbarkeit von Prolin als Biomarker für die Vitamin C-Versorgung genutzt werden. Ein Mangel hingegen von Prolin, Vitamin C, Eisen und Vitamin B6 würde unter anderem den Aufbau von Bindegewebe beeinträchtigen.
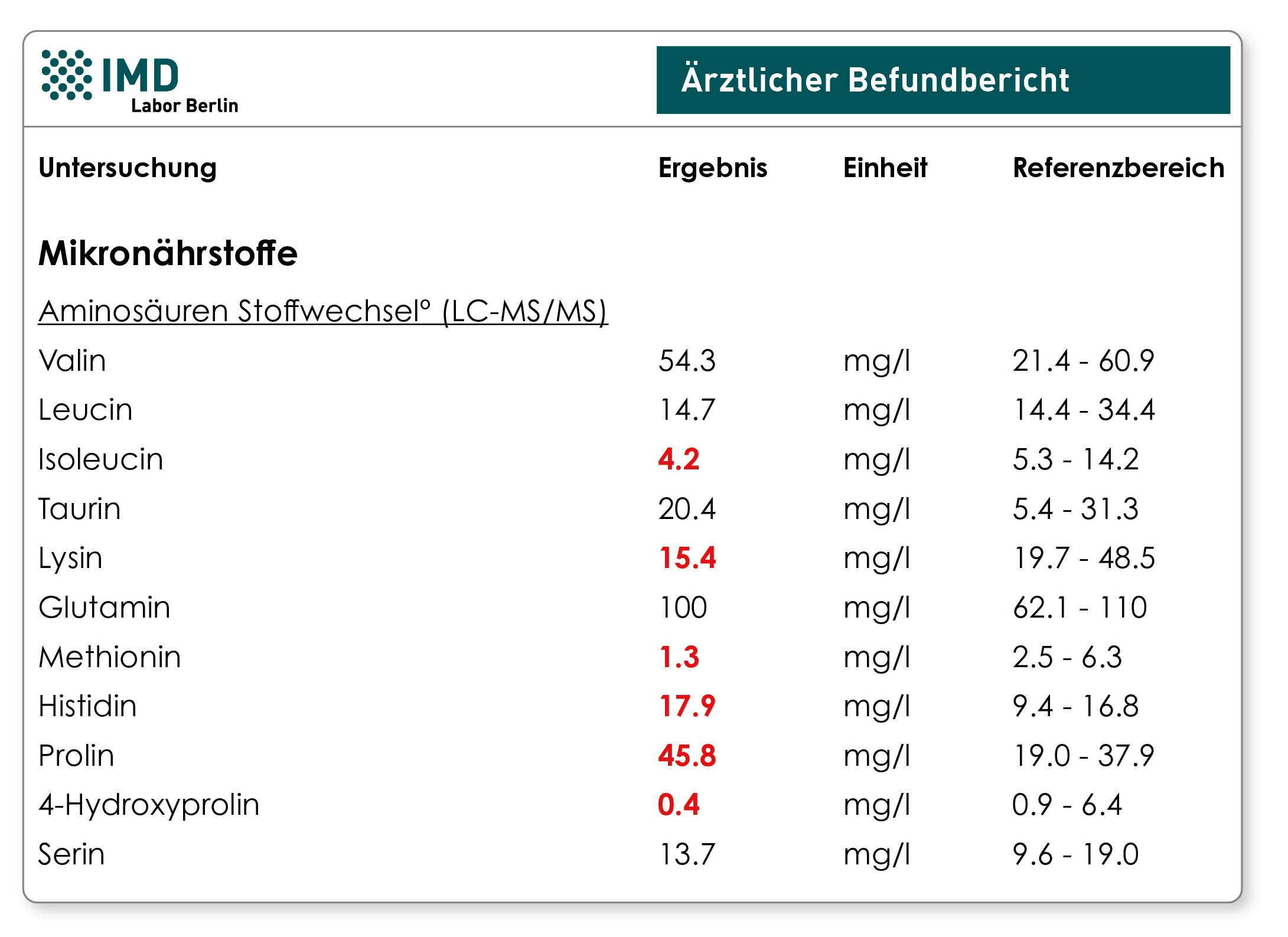
Hyroxyprolin entsteht enzymatisch aus Prolin, Kofaktor: Vitamin C
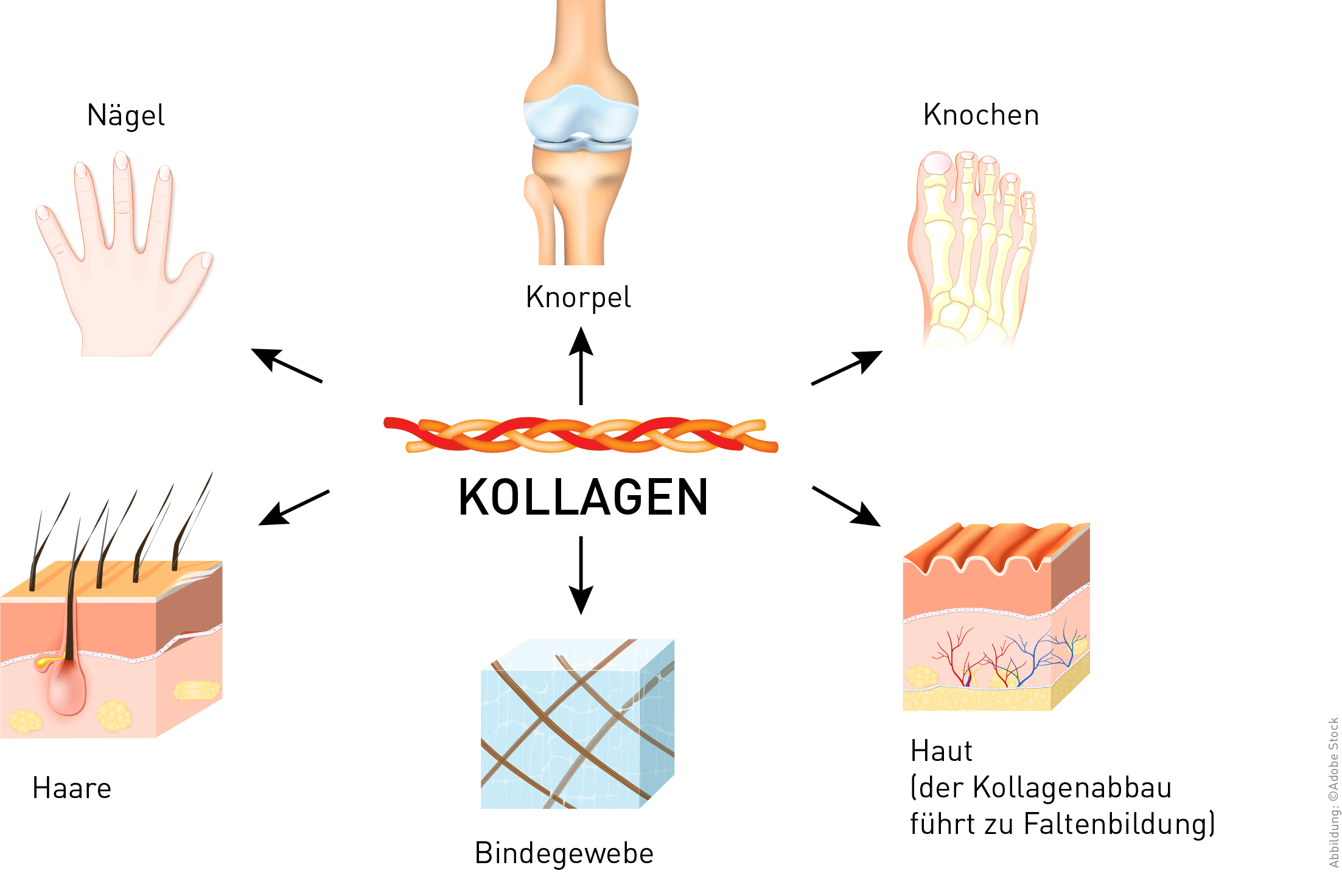
Vitamin C ist als Kofaktor essentiell für die Kollagensynthese. Daher stört ein Vitamin C-Mangel die Bildung von kollagenhaltigem Gewebe wie Haut, Knorpel, Knochen und Bindegewebe.
Die Pharmakokinetik von Vitamin D ist individuell sehr unterschiedlich. Dies beruht vor allem auf folgenden Einflussfaktoren:
Resorption: Vitamin D ist ein fettlösliches Vitamin und sollte daher zu den Mahlzeiten eingenommen werden. Es wird im Wesentlichen im Dünndarm resorbiert. Jegliche Erkrankung des Dünndarms kann daher – trotz adäquater oraler Zufuhr – einen Vitamin-D-Mangel begünstigen. Man sollte insbesondere Erkrankungen wie Zöliakie und chronisch entzündliche Darmerkrankungen ausschließen. Eine erhebliche (gewollte) Verringerung der resorptiven Oberfläche im Dünndarm haben aber auch Patienten mit Z n. bariatrischer Chirurgie. Diese Patienten sind aber insbesondere zur Verbesserung ihrer oft pathologischen Insulinresistenz auf eine adäquate Vitamin-D-Versorgung angewiesen.
Metabolismus: Die Enzyme, die Vitamin D metabolisieren ((25-Hydroxylase, 1-alpha-Hydroxylase und 24-Hydroxylase) kommen beim Menschen in unterschiedlichen Genvarianten vor. Der Summationseffekt dieser Varianten ist entweder eine Verlangsamung oder eine Beschleunigung des Metabolismus und damit eine Verlangsamung oder Beschleunigung des Anstiegs von Vitamin D im Blut nach Substitution. In den letzten Jahren gibt es darüber hinaus Hinweise, dass die Gene, die für den Metabolismus von Vitamin D verantwortlich sind, auch erheblichen epigenetischen Veränderungen unterliegen. Diese tragen ebenfalls zur Variabilität des Konzentrationsanstiegs im Blut nach oraler Vitamin-D-Gabe bei.
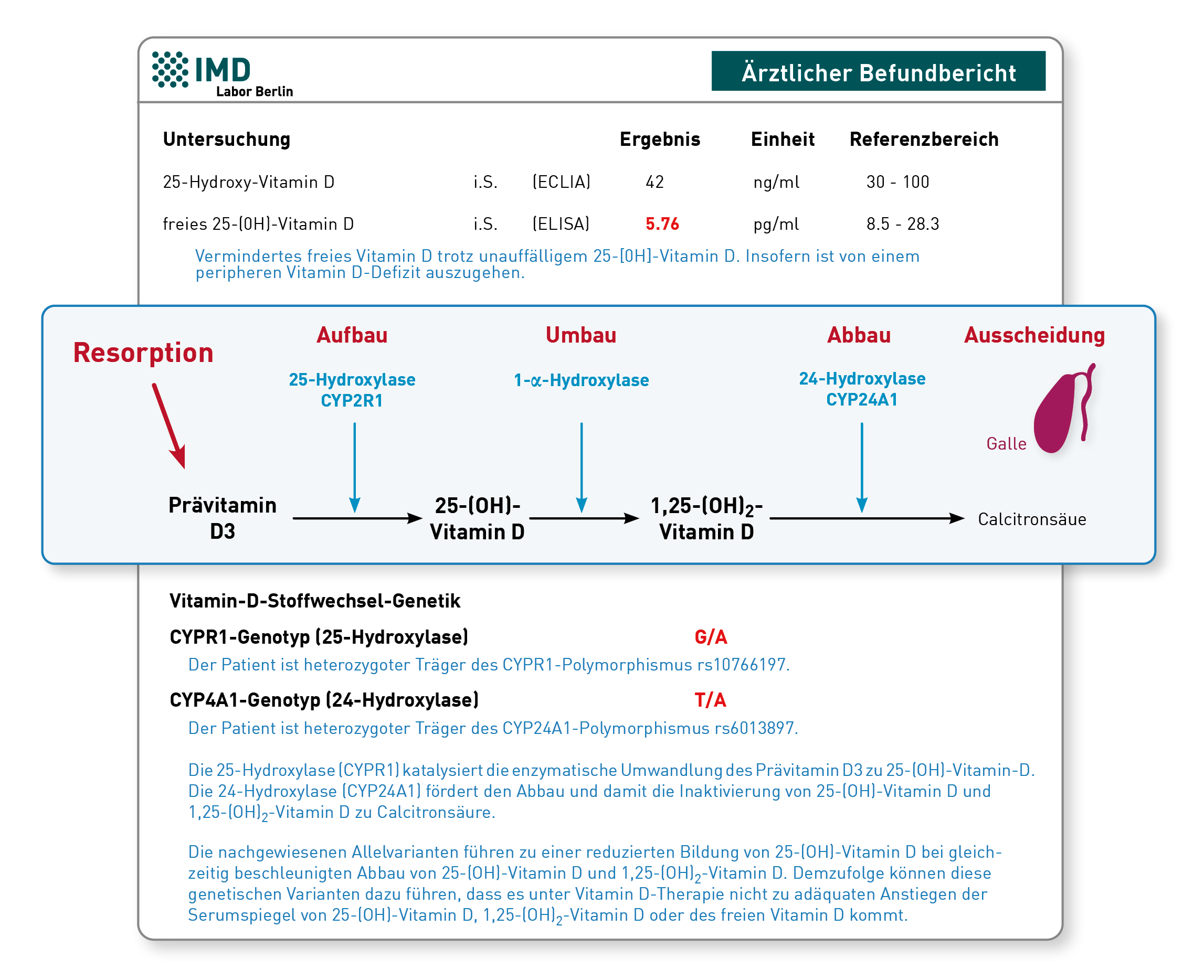
Empfehlung: Aufgrund dieser aus den oben genannten Gründen sehr hohen Variabilität der Vitamin-D-Blutkonzentrationen nach oraler Gabe und der Tatsache, dass sowohl Mangel als auch Überdosierung zu vermeiden sind, schlagen wir ein pragmatisches Vorgehen bei der Vitamin-D-Substitution vor. Beginnen sollte man die Substitution mit Dosen nach den Empfehlungen der jeweiligen Fachgesellschaften. Diese Therapie muss dann aber durch Bestimmung von Vitamin D (das freie 25(OH) Vitamin D ist hier vorzuziehen, da es besser die biologische Aktivität des Vitamin-D-Systems widerspiegelt) überwacht und entsprechend angepasst werden. Feste Schemata ohne Kontrollen sind aufgrund der oben beschriebenen Variabilität der individuellen Antworten zu vermeiden. Die genetische Untersuchung der metabolisierenden Enzyme 25-Hydroxylase (CYP2R1) und 24-Hydroxylase (CYP24A1) sowie des Vitamin-D-Bindeproteins (VDBP) liefern wichtige prognostische Anhaltspunkte.
Grundsätzlich lässt die Entgiftungsgenetik Patienten erkennen, die exogene toxische Substanzen weniger effizient abbauen, schlechter ausscheiden und somit zur Anreicherung von Organbelastungen neigen. Gleichermaßen identifizieren die genetischen Untersuchungen aber Patienten, die endogene, durch Zellstress entstehende reaktive Sauerstoffverbindungen unzureichend eliminieren. Diese lebenslange Risikokonstellation zu erkennen, kann Arzt und Patient bei präventiven Ansätzen (Reduktion der Fremdstoffbelastung, Versorgung mit Antioxidantien u.a.) grundlegend unterstützen. Darüber hinaus ergeben sich jedoch auch spezifische praktische Konsequenzen aus den einzelnen Genveränderungen:
CYP-450-Enzyme: Sie sind für die Phase 1 der Metabolisierung von Fremdstoffen verantwortlich. Genetische Polymorphismen können sich daher nicht nur deutlich auf die Wirksamkeit von Medikamenten auswirken (z.B. CYP2D6 und Antidepressiva), sondern z.B. auch auf die Verfügbarkeit von Vitamin D (bei Veränderung von CYP2R1 und CYP24A1). Die Kenntnis der Genetik kann hier helfen, die Dosierung von Medikamenten und Vitamin D zu verbessern.
GST-Enzyme und NAT2: Durch die Phase-2-Enzyme werden die in Phase 1 entstandenen Metabolite wasserlöslich / ausscheidbar gemacht. Eine genetische Einschränkung der Aktivität der Phase-2-Enzyme führt dazu, dass in der Phase 1 entstehende (z.T. sogar toxischere) Metabolite weniger effizient eliminiert werden. Für betroffene Patienten kann daher die Intensivierung der Phase 1 durch die Gabe hochdosierter Mikronährstoffe (besonders B-Vitamine) problematisch werden. Das wird dann oft als die Unverträglichkeit von B-Vitaminen erlebt. Wichtige Kofaktoren der Phase 2 sind u.a. Glutathion und weitere Aminosäuren und Selen. Labordiagnostisch werden die Kontrolle von Glutathion intrazellulär, Aminosäuren Stoffwechsel und eine Vollblutmineralanalyse empfohlen.
SOD2: Die mitochondriale Superoxiddismutase neutralisiert reaktive Sauerstoffspezies ("Radikale") in Mitochondrien. Patienten mit genetisch bedingt verminderter Enzymfunktion neigen dazu, oxidativen Stress gerade dann insuffizient abzufangen, wenn der mitochondriale Stoffwechsel gesteigert ist und dienen hier auch der Stoffwechselregulation. Dies tritt bei vermehrtem Energiebedarf der Zelle ein, wie z.B. in Immunzellen bei Entzündung oder in Muskelzellen bei körperlicher Aktivität. Radikale werden für Regulationsprozesse benötigt, aber ein Zuviel bedeutet Oxidativen Stress. Dieser schädigt körpereigene Strukturen, daher ist die Balance wichtig. Eine gute Versorgung mit Antioxidantien (Vitamin C, A, E, Coenzym Q10, Taurin aber auch die alpha-Liponsäure) sollte bei Patienten mit SOD-2-Mangel stets gewährleistet sein.
Die u.g. 5 Enzyme sollten hinsichtlich ihrer Genetik gemeinsam betrachtet werden. Eine Kombination genetisch reduzierter Enzymaktivitäten, z.B. der N-Acetyltransferase 2 (NAT2) und der GST´s hat eine größere Bedeutung.
Bei Patienten mit mehrfach auffälligen Polymorphismen, kann mithilfe folgender Mikronährstoffe eine teilweise Kompensation erreicht werden: Glutathion und Selen, Antioxidantien (Vitamin C, A, E, Coenzym Q10, Taurin, alpha-Liponsäure), über eine Verbesserung der Methylierung (Vitamin B12, Folsäure, SAM) kann die „Ablesbarkeit der Gene“ verbessert werden.

Abb.: Eingeschränkte Funktion der Enzyme GST-M1, GST-T1, NAT2 und SOD-2. Dies spricht für einen grundsätzlich erhöhten Bedarf an Antioxidanzien, eine verzögerte Ausscheidung von Metaboliten der Phase 1 (sowie auch Metallen!).
Wichtige Anhaltspunkte liefern das freie 25-OH-Vitamin-D sowie Genvarianten des Vitamin-D-Metabolismus. Ist das freie Vitamin D unter der Substitution in den Normbereich angestiegen und nur das Gesamt-25OH-Vitamin-D niedrig geblieben, spricht diese Konstellation für eine aktuell ausreichende Versorgung. Eine mögliche Erklärung für das trotzdem niedrige Gesamt 25OH-Vitamin-D wäre ein Polymorphismus im Vitamin-D-bindenden Protein (VDBP-Gen), wodurch sowohl die Konzentration als auch die Affinität des VDBP vermindert sein kann. Das würde bedeuten, dass der Patient weniger „Speicher“ anlegen kann. Sowohl die VDBP-Konzentration im Serum als auch die VDBP-Genetik kann im Labor untersucht werden. Falls jedoch auch das freie Vitamin D unter der Substitution erniedrigt bleibt – und Probleme der enteralen Resorption ausgeschlossen sind – kann die Ursache in genetischen Varianten liegen, die den Vitamin-D-Metabolismus stören. So verlangsamt eine Variante des Enzyms CYP2R1 (25-Hydroxylase) die Synthese von 25OH-Vitamin-D aus dem therapeutisch verabreichten Provitamin D. Ein Polymorphismus im CYP24A1-Gen (24-Hydroxylase) wiederum steigert den Abbau von 25OH-Vitamin-D und 1,25-(OH)2-Vitamin-D zur wirkungslosen Calcitronsäure. Daher führen diese Varianten unabhängig voneinander dazu, dass 25OH-Vitamin-D (sowohl Gesamt- als auch freies) trotz Substitution unzureichend ansteigt. Bei Vorliegen beider Genveränderungen wird der Effekt verstärkt. Während die Analytik des freien Vitamin D, der VDBP-Serumspiegel sowie die VDBP-Genetik bereits am IMD verfügbar war, haben wir nun auch die Genetik des Vitamin-D-Metabolismus (CP2R1- und CYP24A1-Gen) validiert. Weitere Hintergründe und Details finden Sie in unserer Diagnostikinformation „Vitamin D-Stoffwechselgenetik“.
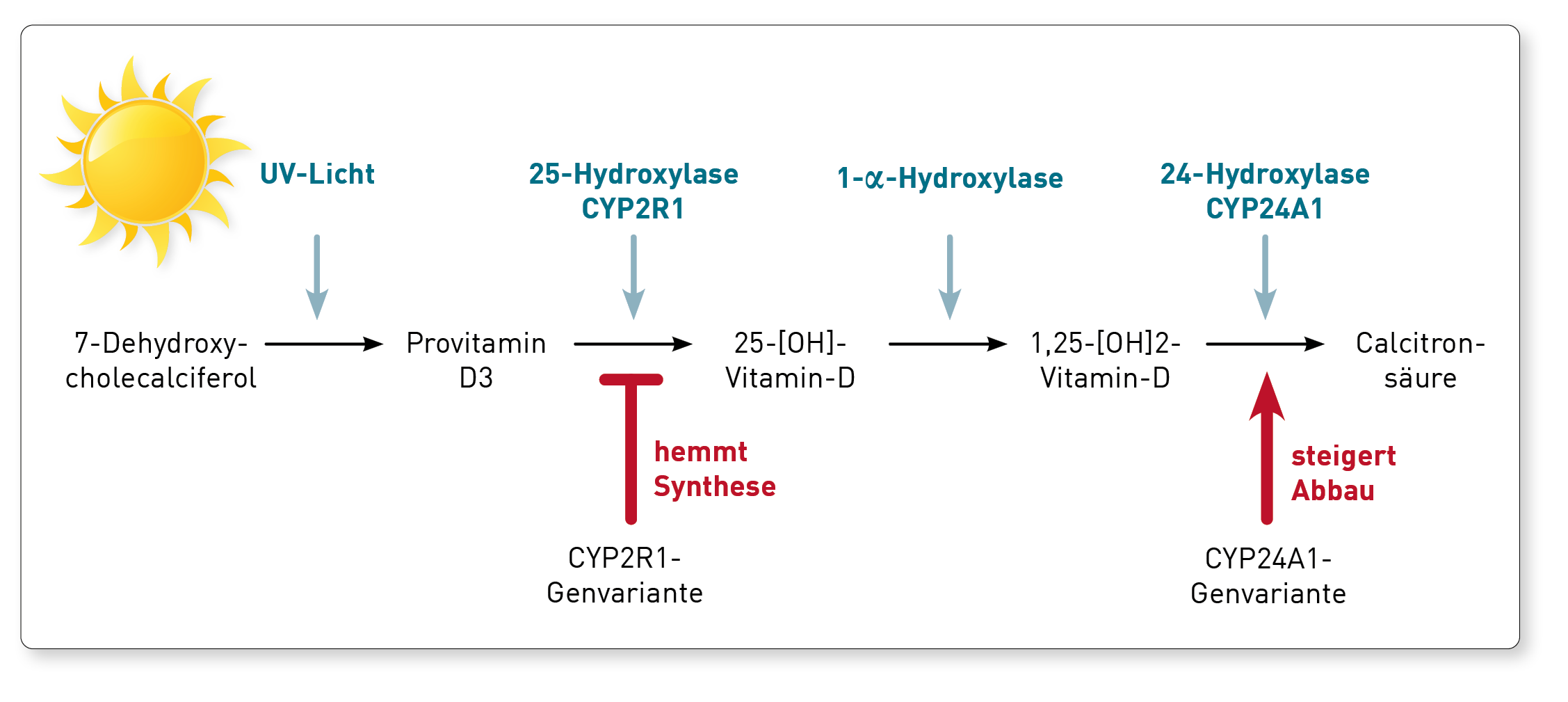
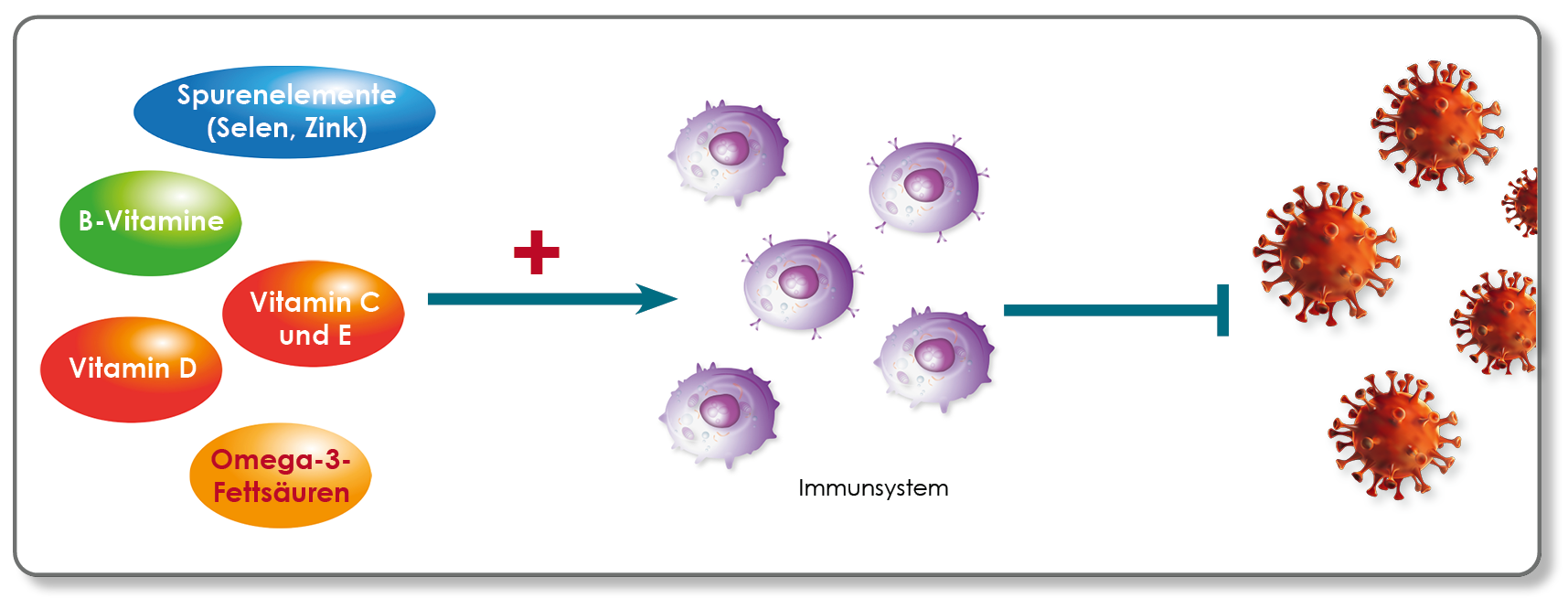
Immunaktivierung steigert den Bedarf an Vitaminen und Spurenelementen. Gleichzeitig kann ein guter Versorgungsstatus nachweislich Infektionsrisiken senken. Studien dieser Art fehlen zwar weitgehend für das Coronavirus SARS-CoV2, einige Mikronährstoffe werden jedoch in der wissenschaftlichen Literatur diskutiert (Zhang et al., Journal of Medical Virology 2020):
- B-Vitamine
Insbesondere B6, aber auch andere B-Vitamine sind wichtige Kofaktoren der mitochondrialen Energiegewinnung und daher essentiell für eine optimale Funktion von Immunzellen. Eine gute Versorgung ist daher essentiell für eine Stärkung der Immunfunktionen. B2 zeigte in vitro eine spezifische Aktivität gegen das Coronavirus MERS-CoV. - Vitamin C
Studien zeigen, dass Vitamin C vor Infektionen der unteren Atemwege schützen kann. In Hühnern wurde zudem eine protektive Rolle gegenüber einem anderen Corona-Virus gezeigt. - Vitamin D
Aufgrund seiner weit reichenden Bedeutung für das Immunsystem vermutet man, dass eine gute Vitamin D-Versorgung auch für die Abwehr von SARS-CoV2 förderlich ist. In Kälbern wurde gezeigt, dass Infektionen mit einem bovinen Coronavirus durch Defizienzen an Vitamin D und E begünstigt werden. - Selen
Eine ausreichende Selenversorgung ist von zentraler Bedeutung für die Immunfunktion. Tiermodelle zeigen darüber hinaus spezifische schädigende Effekte eines Selenmangels, wie eine Verstärkung des Krankheitsverlaufes bei Influenza, sowie eine Steigerung der Virulenz verschiedener Erreger durch erhöhte Mutationsrate im Virusgenom. Von einer exzessiven, unkontrollierten Zufuhr ist angesichts der Corona-Epidemie dennoch abzuraten, da Selenverbindungen einem Bericht zufolge den ACE2-Rezeptor, das Eintrittstor von SARS-CoV2 in die Zelle, hochregulieren könnten. - Zink
Zink wird für die Differenzierung von T-Zellen benötigt, ein Vorgang, der essentiell ist für die Abwehr von akuten Infekten. Darüber hinaus wurden spezifische Interaktionen mit verschiedenen viralen Erregern belegt. So hemmt intrazelluläres Zink die Replikation verschiedener RNA-Viren, u.a. auch die des „ersten“ SARS-Virus (SARS-CoV). - Omega-3-Fettsäuren
In Tiermodellen wurden protektive Effekte von Omega-3-Fettsäuren gegenüber Influenza und Hepatitis C-Viren beobachtet. Der Versorgungsstatus der aufgeführten Mikronährstoffe kann sowohl über gezielte Einzelanalysen als auch im Rahmen von Diagnostikprofilen als bioaktive B-Vitamine, Vollblutmineralanalysen, Fettsäuren der Erythrozytenmembran untersucht werden. Bitte beachten Sie auch unser neues Profil „Vitalstoffe Infektneigung“ (Selen, Zink, Glutathion, Vitamin D, siehe 6-seitiger Schein).
Nach aktuellen Erkenntnissen kann eine gute Mikronährstoffversorgung der Krankheitsprogression und der Entstehung typischer Komorbiditäten wie Arteriosklerose, Hypertonus, Retinopathie und Neuropathie entgegenwirken. Folgende Zusammenhänge sind von besonderer therapeutischer Relevanz:
- Vitamin D fördert die Insulinsekretion der Beta-Zellen und wirkt damit der Insulinresistenz entgegen.
- Eine ausreichende Mineralstoffversorgung ist für die Funktion des Insulinsignalweges essentiell. So dient Mangan als Kofaktor der Insulinsynthese und -sekretion. Magnesium und Chrom unterstützen die Bildung und Funktion des Insulinrezeptors.
- Diuretika-Gaben gehen oft mit Mineralstoffverlusten einher. Auch Zink mit seinen vielfältigen Funktionen ist bei Diabetikern häufig nicht ausreichend vorhanden.
- Statine können die Spiegel an Selen und Coenzym Q10 senken und daher oxidativen Stress verstärken, der sowohl arteriosklerotische als auch neurodegenerative Veränderungen fördert.
- Omega-3-Fettsäuren sind notwendig für die Regeneration von Nervenzellen. Alpha-Liponsäure als potentes Antioxidans und natürlicher Metallchelator kann in der Prävention von Diabetes-assoziierten Neuropathien eingesetzt werden.
- Die Entstehung neuropathischer Veränderungen wird auch durch den bei Diabetikern häufigen Vitamin B1-Mangel gefördert, da Vitamin B1 am Aufbau von Myelin und an der Regeneration von Nervenzellen beteiligt ist. Die neuronale Regeneration wird ferner von Vitamin B12 unterstützt, das bei Einnahme von Metformin häufig defizient ist.
- Gleichzeitig blockiert Metformin den Komplex I der mitochondrialen Atmungskette und hemmt dadurch die ATP-Synthese. Zur Verbesserung der Mitochondrienfunktion sollte daher an eine ausreichende Versorgung mit Vitamin B3 und Coenzym Q10 gedacht werden.
Zur Untersuchung der spezifisch bei Typ II Diabetes wichtigen Mikronährstoffe werden wir zukünftig auf dem neuen, 6-seitigen Anforderungsschein das Profil „Vitalstoffe Diabetes“ anbieten (Profilinhalt: HbA1c, freies Vitamin D, Vitamin B1, B3, B12 bioaktiv, Q10, Alpha-Liponsäure, Carnitin, Chrom, Magnesium, Mangan, Selen, Zink). Ferner empfehlen wir Homocystein sowie die Fettsäuren der Erytrozytenmembran zu bestimmen. Bis zur Verfügbarkeit des 6-seitigen Scheines (Mitte März 2020) bitten wir Sie, die Profilinhalte einzeln anzufordern.
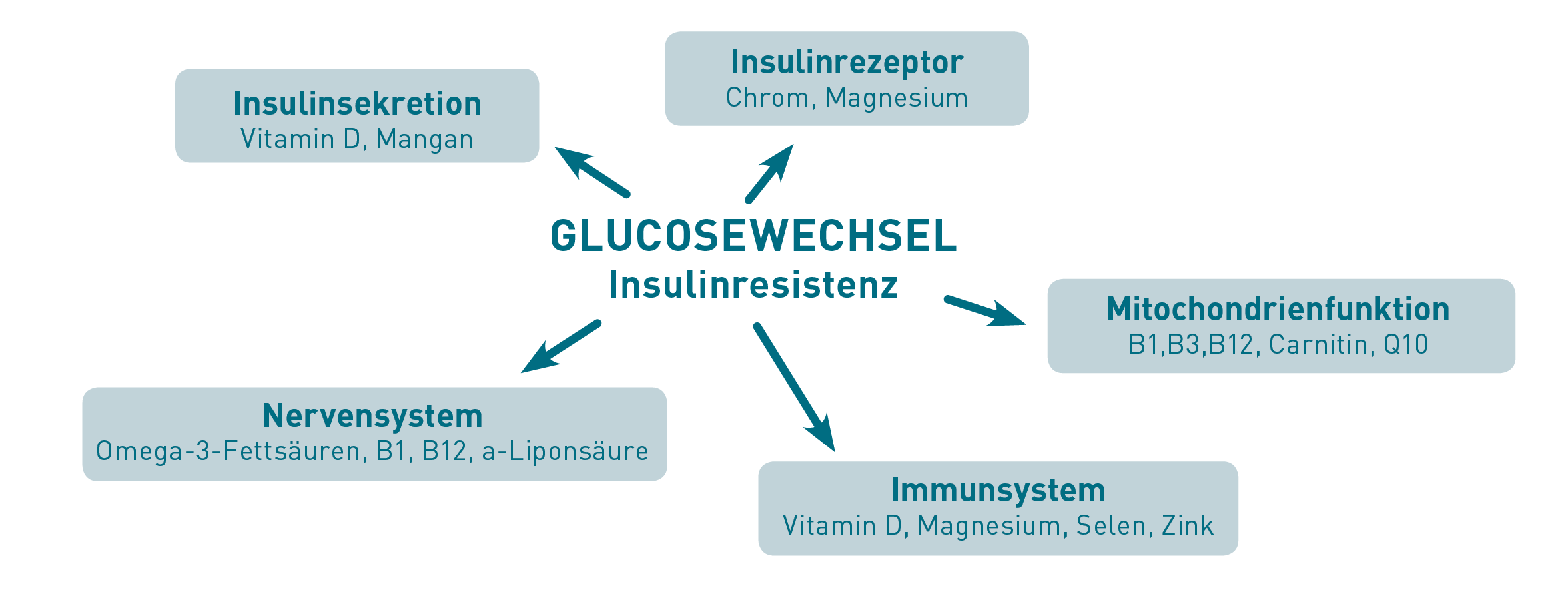
„Eisen im Vollblut“ eignet sich genauso wenig wie Eisen im Serum zur Beurteilung des Eisenstatus. Das im EDTA- oder Heparinvollblut gemessene Eisen stammt zu 99 % aus dem Hämoglobin – seine Aussagekraft ist daher nicht besser als die des Hb-Wertes. Dieser ist aufgrund der 3-monatigen Lebensdauer der Erythrozyten nicht geeignet, Unterversorgungen mit verfügbarem Eisen frühzeitig zu erkennen. Ein Abfall des Hb und des Vollblut-Eisens wird erst bei einer Eisenmangelanämie beobachtet, also bei fortgeschrittenem, klinisch manifestem Eisenmangel. Die Messung von Eisen in der Vollblutmineralanalyse birgt die Gefahr, dass die Eisenzufuhr anhand dieses wenig sensitiven Parameters beurteilt wird und Defizienzen unerkannt bleiben. Aus diesem medizinischen Grund haben wir uns entschieden, Eisen nicht in den Mineralstoffprofilen des IMD mit zu messen, auch wenn es methodisch ganz und gar unproblematisch wäre. Zur verlässlichen und sensitiven Kontrolle der Eisenversorgung empfehlen wir stattdessen die Anforderungen Ferritin, hsCRP, löslicher Transferrinrezeptor und Ferritinindex (auch als Kassenleistung möglich). Der Ferritinindex wird aus Ferritin und dem löslichen Transferrinrezeptor errechnet und ermöglicht die Beurteilung des Eisenstatus auch bei entzündungsbedingtem Ferritinanstieg. Ausführliche Hintergründe zur Diagnostik des Eisenstoffwechsels finden Sie in unserer Diagnostikinformation.
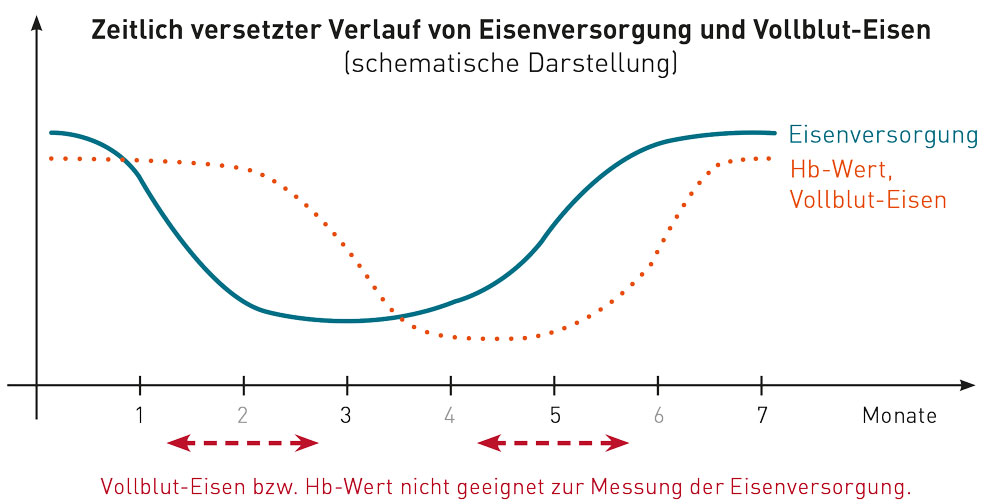
Die herkömmliche Blutspiegelanalyse von Vitamin K2 ist aus präanalytischen Gründen und wegen der starken nahrungsabhängigen Schwankungen ungeeignet, um die Vitamin K2-Versorgung einzuschätzen. Ein erhöhtes ucOsteocalcin zeigt einen Mangel an Vitamin K2 besser an. Der Anstieg des ucOsteocalcins beruht dabei darauf, dass K2-Mangel die Carboxylierung des ucOsteocalcins hemmt. Aus diesem Grund steigt bei Vitamin K2-Mangel das untercarboxylierte („uc“) Osteocalcin im Blut an und ist stabil messbar.
Ein normwertiges oder vermindertes ucOsteocalcin zeigt eine ausreichende Versorgung mit Vitamin K2 an. In den seltenen Fällen eines verminderten ucOsteocalcins empfiehlt sich eine weiterführende Diagnostik:
• Mögliche Ursache für erniedrige Werte ist eine Störung des Knochenstoffwechsels, z. B. aufgrund von Vitamin D-Mangel, denn Vitamin D aktiviert die Sekretion von ucOsteocalcin aus den knochenbildenden Osteoblasten.
• Alternativ könnte Vitamin K2 besonders hohe Aktivität haben, so dass die Carboxylierung vermehrt
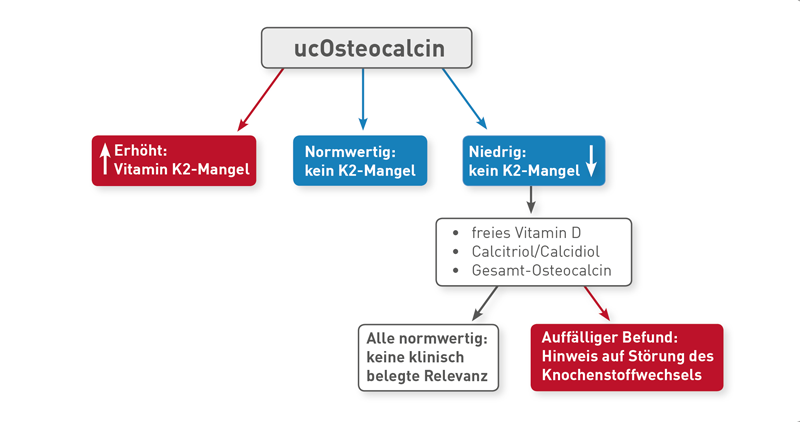
Wir empfehlen die „Folsäure bioaktiv“. Bereits die Bezeichnung „intrazellulär“ ist grundsätzlich irreführend, da hier in den Laboren lediglich der Blutkuchen untersucht wird. Dieser besteht zu 99 % aus Erythrozyten, die als „Transporthüllen“ des Hämoglobins weder über Zellkern noch über Mitochondrien und andere Organellen verfügen. Ihr Stoffwechsel und ihr Bedarf an Mikronährstoffen sind daher nicht mit echten Zellen gleichzusetzen. Richtig wäre, wenn man die Analyse „Folsäure intraerythrozytär“ nennen würde. Ferner misst die Erythrozyten-Analyse analog zur konventionellen Serumanalyse lediglich die Folsäure-Konzentration. Die Konzentrationsbestimmung erfasst dabei üblicherweise die Folsäure und zwei Folsäure-Metabolite (5-Methyl- und 5-Formyl-Tetrahydrofolat).
Daher erfasst die Spiegelbestimmung (in Erythrozyten wie im Serum) weder die zahlreichen weiteren bioaktiven Folsäure-Metabolite noch ihre anteilige Verteilung. So kann ein geringer Anteil an 5-Methyl-THF dazu führen, dass trotz normwertigem Spiegel die Folsäure-Bioaktivität vermindert ist (siehe Abbildung). Nur bei ausreichender Bioaktivität steht jedoch „Folsäure“ als Mikronährstoff dem Stoffwechsel in ausreichender Menge zu Verfügung.
Es ist bisher keine Methode verfügbar, Folsäure-Bioaktivität in Erythrozyten zu messen – oder gar in Leukozyten, die als echte Zellen repräsentativer für Körperzellen wären. Deshalb empfehlen wir die Bestimmung der „bioaktiven Folsäure im Serum“ als den derzeit aussagefähigsten Marker für den Folsäure-Status (Analyse 106, Schein „Spezielle Immunologie“).

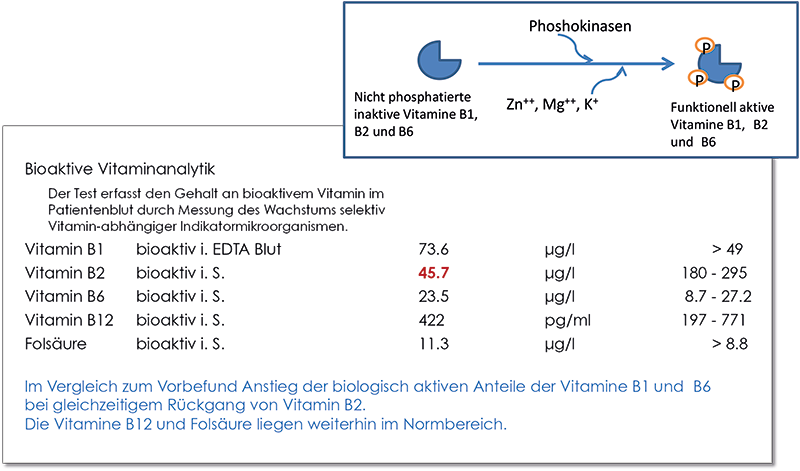
Vitamin B1, B2 und B6 entfalten ihre Wirksamkeit erst nach ihrer Umwandlung in Thiamin-, Riboflavin- und Pyridoxal-Phosphate. Diese Biotransformation geschieht enzymatisch über die Anlagerung von Phosphaten mit Hilfe verschiedener Phosphokinasen. Der Anstieg der Bioaktivität hängt damit nicht allein von der supplementierten Dosis ab, sondern auch von der Effizienz der Biotransformation. Die zentralen Enzyme, so genannte Phosphokinasen, weisen eine individuell unterschiedliche Aktivität auf, wozu vermutlich genetische Faktoren beitragen. Gleichzeitig wird die Rate der Biotransformation durch die Verfügbarkeit von Spurenelementen beeinflusst, insbesondere von Zink, Magnesium und Kalium.
Hinzu kommt, dass in Abhängigkeit der Aktivität einzelner Stoffwechselprozesse die verfügbaren B-Vitamine unterschiedlich stark „verbraucht“ werden. Diese Vitamin-abhängigen Vorgänge werden durch Supplementierung unterstützt und oft beschleunigt. Zum Beispiel braucht die Pyruvatdehydrogenase Vitamin B1, verschiedene Schritte des Zitratzyklus wiederum benötigen die Vitamine B2 und B6. Die erfolgreiche Behandlung eines Nitrosativen Stress (erkennbar am Abfall des Nitrotyrosins im Blut) steigert z. B. die Aktivität der Pyruvatdehydrogenase und damit sekundär den Bedarf an Vitamin B1.
Der oben genannte Verlauf könnte damit erklärt werden, dass verabreichtes Vitamin B6 mit Hilfe von Zink, Magnesium, ATP und Vitamin B2 zu aktiven Vitamin B6-Formen metabolisiert wird. Die Biotransformation von Vitamin B6, vor allem über das Enzym Pyridoxin 5‘-phosphatoxidase, verbraucht also Vitamin B2. Daher kann es durch den substitutionsgeförderten Anstieg der Vitamin B6-Aktivität vorübergehend zu einem Abfall des bioaktiven Vitamin B2 kommen. In seltenen Fällen geschieht dies auch bei Supplementierung mit Pyridoxal-5-Phosphat (P-5-P) – dann vermutlich aufgrund unvollständiger Phosphatierung bzw. Oxidierung des Supplements. Häufig ist jedoch ein schnellerer Anstieg des bioaktiven Vitamin B6 zu beobachten, wenn P-5-P verwendet wird.
Wir empfehlen für die Untersuchung der Spurenelemente immer die Vollblutmineralanalyse (im EDTA- oder Heparin-Vollblut). Sie erfasst die Gesamtheit der Spurenelemente, die über das Blut ans Gewebe verteilt werden. Bei der Vollblutmineralanalyse untersuchen wir das Blut als „Transportmedium“ für die Gewebeversorgung. Die Analytik beantwortet die Frage: Stehen den Organen und Geweben ausreichende Mengen an Mineralstoffen zu Verfügung?
Nicht sinnvoll hingegen ist die Analyse von Mineralstoffen in isolierten Fraktionen des Blutes (PBMCs oder Erythrozyten), wenn es um den Versorgungsstatus des Patienten geht. Es gibt hier z. B. entzündungsabhängige Verschiebungen, die nichts mit dem Versorgungsstatus zu tun haben (u. a. den Einstrom von Calcium – daher messen wir das Calcium in Leukozyten im Rahmen chronisch entzündlicher Veränderungen). Auch eine Gleichsetzung von Erythrozyten mit Gewebezellen ist nicht zulässig – Erythrozyten haben keinen Zellkern und keine Mitochondrien, ihr Stoffwechsel und damit auch ihr Mikronährstoffbedarf ist daher in keiner Weise mit dem Stoffwechsel echter Zellen vergleichbar.
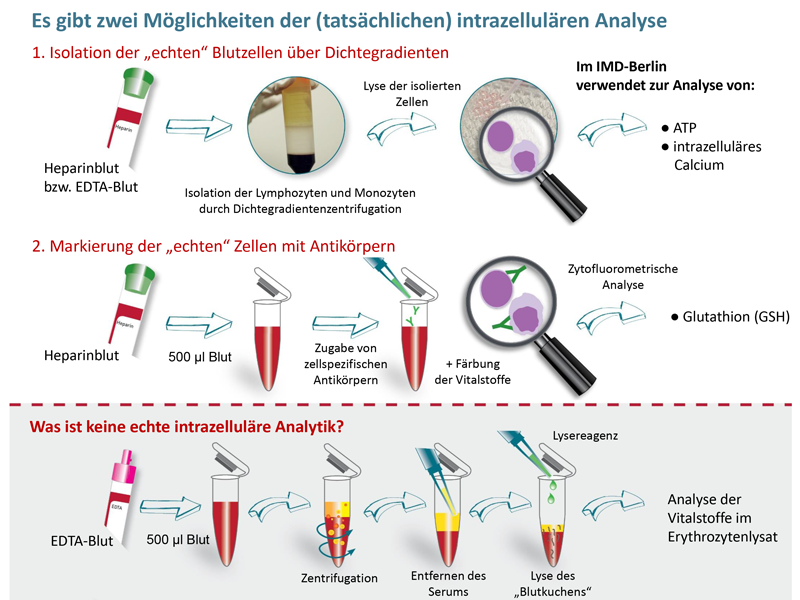
Anders ist das bei den intrazellulär gebildeten Vitalstoffen wie ATP und Glutathion, die im Februar-Newsletter dargestellt wurden. Sie werden nicht wie Spurenelemente über das Blut verteilt, sondern sie werden in allen (echten) Zellen gebildet. Daher bietet ihre Bestimmung in echten Zellen (im Blut wären das die so genannten PBMCs) die Möglichkeit, auf andere Gewebezellen rückzuschließen.

Abb. Die Vollblutmineralanalyse erfasst die Gesamtheit der über das Blut an die Organe verteilten Spurenelemente. Sie ist daher maßgeblich für die Beurteilung des Versorgungsstatus. Im Blut besteht ein Austausch zwischen freien, proteingebundenen und intrazellulären (Erythrozyten, Leukozyten) Spurenelementen.
Für die Beurteilung des Versorgungsstatus und ggf. des Substitutionsbedarfes an Vitalstoffen wie z. B. Spurenelementen, Vitaminen, ATP oder Glutathion ist die Einschätzung der Gewebeversorgung maßgeblich. In der Praxis steht uns jedoch als Untersuchungsmaterial ausschließlich das Blut zu Verfügung. Generell gilt, dass die Aussagekraft der Laborwerte größer ist, wenn man nicht nur die frei im Blutserum enthaltenen Stoffe sondern auch die intrazellulären Anteile erfasst.
Für die Untersuchung der Spurenelemente liefert die Vollblutmineralanalyse die aussagekräftigen Laborwerte, da sie sowohl die intrazellulären Pools als auch den Serumanteil erfasst, der für den Transport in Organe und Gewebe zu Verfügung steht. Die Vollblutmineralanalyse zeigt an, ob für die physiologisch regulierte Verteilung ins Gewebe ausreichend Spurenelemente vorhanden sind.
Andere Vitalstoffe werden nicht an Gewebe und Organe verteilt, sondern in den Zellen gebildet, wie z. B. ATP und Glutathion. Zur Bestimmung ihres Versorgungsstatus sollte deshalb ihr Gehalt auch ausschließlich in Blutzellen gemessen und davon der Versorgungsstatus der Gewebezellen abgeleitet werden.
Dabei wird der Terminus „intrazellulär“ oft missverständlich verwendet. Unter „intrazellulär“ verstehen wir die Bestimmung in Monozyten und Lymphozyten, die auch als PBMC (Peripheral Blood Mononuclear Cells) bezeichnet werden. PBMC sind „echte“ Zellen, da sie über Zellkern und Mitochondrien verfügen und einen Zellstoffwechsel unterhalten. Nur diese echten Blutzellen sind den Gewebezellen ähnlich genug, um von ihrem Gehalt an Vitalstoffen mit ausreichender Genauigkeit auf die Gewebezellen zurückzuschließen. Erythrozyten stellen hingegen im Wesentlichen die „Transporthülle“ für das Hämoglobin dar. Ein Rückschluss von Erythrozyten auf den Vitalstoffgehalt von Organen und Gewebe ist unzulässig.
Es gibt zwei Verfahren zur intrazellulären Messung:
1. Die Lymphozyten und Monozyten werden aus Heparinblut zuerst durch eine Dichtegradientenzentrifugation von den Erythrozyten, Granulozyten und Thrombozyten sowie vom Serum getrennt (siehe Abb.). Wir verwenden diese Methode für die Bestimmung des ATP, sowie für Calcium, Kalium und Magnesium im Rahmen der Vitamin D-Stoffwechsel-Diagnostik nach Dr. Löffler.
2. Bei der zweiten Möglichkeit zur intrazellulären Analyse werden die Lymphozyten und Monozyten durch Zugabe von zellspezifischen monoklonalen Antikörpern zytofluorometrisch von den restlichen Blutzellen und den Erythrozyten getrennt. Die Anwendung dieser Methode ist dann möglich, wenn auch der zu bestimmende Analyt durch intrazelluläre zytofluorometrisch auswertbare Färbung nachweisbar ist. Wir nutzen diese Methode für die Bestimmung von reduziertem Glutathion (GSH).
Irreführend ist es dagegen, wenn solche Analysen als „intrazellulär“ bezeichnet werden, bei denen aus einer EDTA-Blutprobe lediglich nach Zentrifugation das Serum abgetrennt wird und anschließend der gesamte „Blutkuchen“ zur Analyse verwendet wird. Hier wird der Messwert im Wesentlichen durch die zellkernlosen Erythrozyten und die kurzlebigen Granulozyten bestimmt, die kaum eine Aussage über den Gewebegehalt an Vitalstoffen machen können. Auch ist eine vollständige Entfernung des Serums nicht möglich. Richtigerweise sollte diese Methode wegen der Dominanz der roten Blutzellen immer als „intraerythrozytäre“ Analyse gekennzeichnet werden, wobei wir eine Vitalstoffbestimmung in roten Blutzellen für genauso wenig aussagefähig halten wie die Bestimmung im Serum.
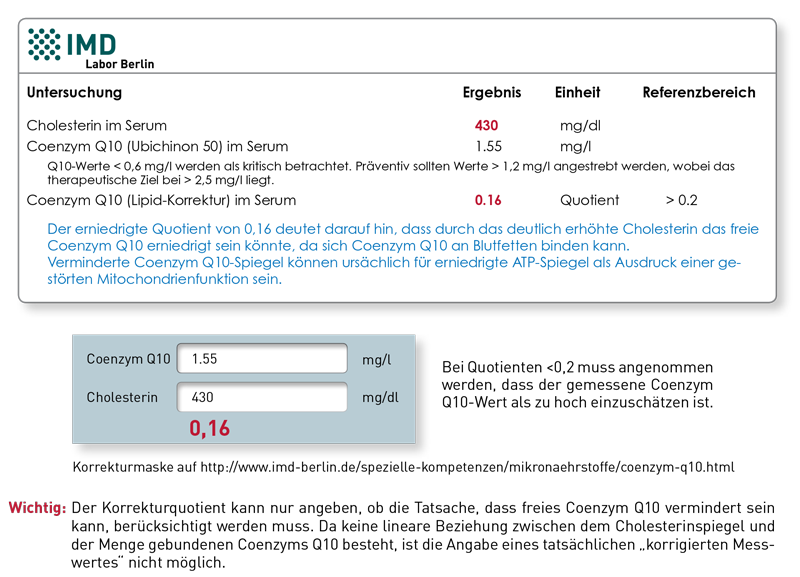
Die Korrektur erfolgt nicht routinemäßig, kann aber auf Wunsch durchgeführt werden. Coenzym Q10 kann mit praktikablen Laborverfahren nur im Serum und nicht intrazellulär bestimmt werden. Üblicherweise findet sich aber eine gute Korrelation zwischen Q10 im Serum und den intrazellulären Spiegeln.
Coenzym Q10 bindet sich im Blut an Cholesterin. Deutlich erhöhte Cholesterinwerte können somit eine normale Coenzym Q10-Versorgung vortäuschen, da dann der Serum-Q10-Wert nicht zwingend mehr den intrazellulären Gehalt widerspiegelt. Deshalb wird von einigen Laboren die Korrektur an Hand des Cholesterinwertes als „unbedingt notwendig“ beworben. Wir empfehlen die Berichtigung dieses Phänomens auch, allerdings nur bei Cholesterinwerten über 350 mg/dl. Bei der zu Grunde liegenden Berechnungsformel kann erst bei Cholesterinwerten > 350 mg/dl oder höher ein grenzwertig normaler Coenzym Q10-Wert auch zu einem pathologischen Lipid-korrigierten Q10-Quotient von < 0,2 führen. Bei normalen Cholesterinspiegeln oder auch therapeutisch normalisierten Werten (z. B. unter Statintherapie) kann die Korrektur sogar fälschlich eine gute Q10-Versorgung vortäuschen. Dieses ist gerade deshalb fatal, weil die Gabe von Statinen nicht nur die Cholesterin-, sondern auch die Coenzym Q10-Synthese hemmt.
Sollten Sie die Lipid-Korrektur der Coenzym Q10-Werte ihrer Patienten auf dem Befund wünschen, vermerken Sie dieses bitte auf dem Anforderungsschein. Andernfalls haben Sie auf unserer Homepage auch die Möglichkeit, in Kenntnis des Coenzym Q10-Wertes die Lipidkorrektur selbst vorzunehmen, z. B. anhand der in Ihrem Hauslabor ermittelten Cholesterinwerte. Die entsprechenden Umrechnungsformeln und eine Umrechnungshilfe finden Sie hier.
Mehr zu diesem Thema finden Sie auf unserer Diagnostikinformation Nr.: 300
Für alle Einsendungen innerhalb von Berlin (d. h. bei denen wir die Proben innerhalb von 6 h im Labor verarbeiten)verwenden auch wir die Spezialröhrchen mit saurem Citrat als Antikoagulanz. Wenn das Blut aber länger als 6h zu uns unterwegs ist (d. h. immer wenn die Proben über Nacht per Kurier zu uns kommen), sind diese Spezialröhrchen keine Hilfe.Auch in diesem Blutröhrchen beginnt nach ca. 6h die Hämolyse von Erythozyten, weshalb es zum artifiziellen Anstieg von Homocystein kommt, welches aus Erythrozyten freigesetzt wird. Das bedeutet,dass Blutproben, die länger als 6h gelagert werden,unabhängig vom verwendeten Röhrchen in jedem Fall innerhalb weniger Stunden nach Blutabnahme zentrifugiert werden müssen und das Plasma/Serum in ein neues Röhrchen übernommen werden muss.Wenn das korrekt erfolgt, sind die Homocysteinwerte für beide Röhrchen identisch. Erfolgt die Zentrifugation aber nicht, messen wir am Folgetag aus beiden Röhrchen falsch hohe Werte.Um nicht erst den Eindruck zu vermitteln, dass man mit dem Spezialröhrchen vielleicht doch auch ohne Zentrifugation einigermaßen korrekte Werte erhält,verzichten wir bei Übernacht-Einsendungen zur Sicherung einer verlässlichen Präanalytik von vornherein auf diese Spezialröhrchen und führen die Analyse bei Übernachteinsendungen nur aus zentrifugiertem und korrekt vom Blutkuchen getrenntem Serum oder Plasma durch. Falsche niedrige Werte durch die Lagerung sind im übrigen nicht zu erwarten, da Homocystein sehr stabil ist.

Warum wird die Vollblutanalyse der Spurenelemente in Ihrem Labor ? nicht auf den Hämatokrit bezogen?
Die Vollblutmineralanalyse untersucht den Versorgungsstatus des Patienten mit essentiellen Spurenelementen. Diese Mineralstoffspiegel werden sinnvollerweise im Gesamt-Vollblut bestimmt, d. h. es werden die intra- und extrazellulären Spurenelemente erfasst. Eine "Normalisierung" auf den Hämatokrit findet dabei am IMD Berlin bewusst nicht automatisch statt, sondern nur auf besonderen Wunsch.
Strikt gegen die Hämatokritkorrektur spricht aus unserer Sicht die Gefahr, dass ein Mineralstoffmangel bei verminderten Erythrozytenzahlen im Blut (v. a. bei Anämie) unerkannt bleiben könnte. Außerdem sind viele Spurenelemente - wie z. B. Selen und Kupfer - intra- und extrazellulär lokalisiert und ihre Verteilung differiert von Patient zu Patient.
Die „Normalisierung“ der Werte anhand des Hämatokritwertes würde hier das Ergebnis verfälschen und einen Mangel möglicherweise „kaschieren“ (siehe Beispielbefund unten). Daher haben wir uns für die herkömmliche Angabe der Blutspiegel in μg/L bzw mg/L entschieden, wenn es um die Beurteilung des Versorgungsstatus mit Mineralstoffen geht.

Mehr zu diesem Thema finden Sie auf unserer Diagnostikinformation Nr.: 298
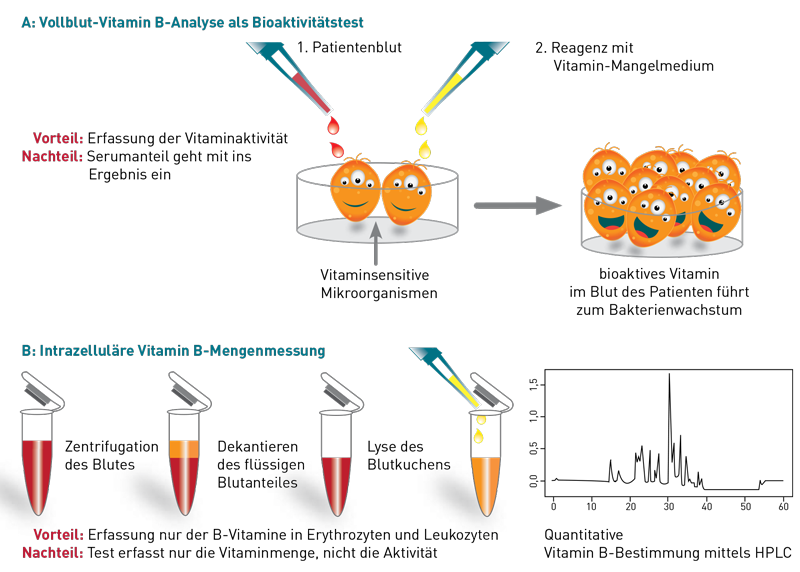
Bei der intrazellulären Analyse der Vitamine B1, -B2 und -B6 wird mittels HPLC die Stoffmenge der Vitamine bestimmt. Es ist dieselbe HPLC-Analyse wie bei der herkömmlichen Vitaminanalytik im Blut, nur dass hier vor der Analyse das Serum abgetrennt wird und nur der Blutkuchen in den Test eingeht. Somit werden die B-Vitaminspiegel in Erythrozyten und geringerem Umfang in Leukozyten bestimmt.
Bei der Analyse Vitamin B1, B2 und B6 Bioaktivität (ID-Vit®-Test) wird die Aktivität der Vitamine bestimmt. Dazu werden alle Zellen der Blutprobe lysiert und in eine Mikrotiterplatte gegeben, die mit vitaminsensitiven Mikroorganismen beschichtet sind. Das für jedes Vitamin individuell zusammengesetzte Medium enthält alle für ein Wachstum der Mikroorganismen notwendigen Bestandteile mit Ausnahme des jeweils zu messenden Vitamins. Nach Zugabe des Patientenblutes wachsen die Mikroorganismen solange, bis das Vitamin aufgebraucht ist. Die Menge an bioaktivem Vitamin des Patienten ist dabei direkt proportional zum Wachstum der Mikroorganismen.
Die Indikationsstellung einer Vitamin-Substitution und die Erfolgskontrolle sollte sich an der Bioaktivität ausrichten und nicht am Substanzspiegel. Der Vorteil der Aktivitätsmessung überwiegt gegenüber dem Fakt, dass hier neben dem zellulären (v. a. erythrozytären) Anteil auch der geringe Gehalt des Serums eingeht.
Der einzige tatsächliche Nachteil der Bioaktivitätsanalyse ist, dass der ID-Vit®-Test aufgrund seiner höheren Kosten keine GKV-Kassenleistung ist und als IGeL-Leistung abgerechnet wird (Kosten 33,22 € je Vitamin). Für Privatpatienten sind die Kosten pro Vitamin aber immer identisch, da die Abrechnungsziffern nicht zwischen Serum, intrazellulärer oder Bioaktivitätsmessung unterscheiden.
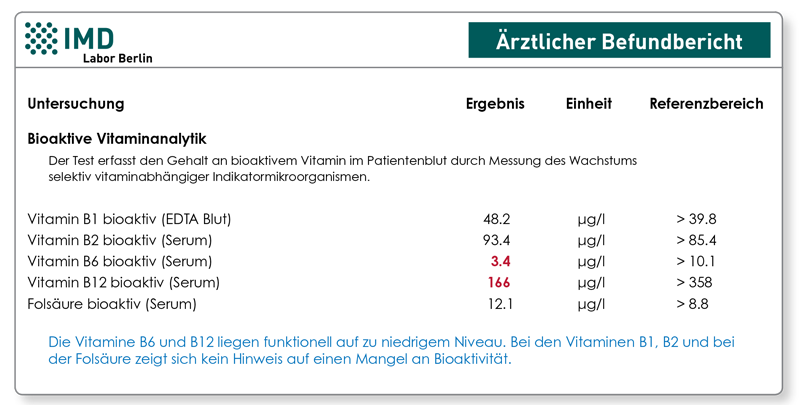
Wir führen die Vitaminbestimmung mit der Bioaktivitätsmethode bei den Vitaminen B1, -B2, -B6 und –B12 sowie bei der Folsäure durch.
Es ist allgemein sinnvoll bei Vitaminen, wo die Vitaminzufuhr einschließlich der therapeutischen Substitution mit Prä-Vitaminen (pro drugs) erfolgt, die von körpereigenen Enzymen erst noch aktiviert werden müssen.
Es betrifft aber auch die Vitamine, die im Blut als unterschiedliche vitaminwirksame Derivate vorliegen. Zum Beispiel stellt Vitamin B6 einen Mix aus 6 interkonvertiblen Substanzen dar, namentlich Pyridoxal (PL), 1-Pyridoxin (PN), Pyridoxamin (PM), Pyridoxal-5-phosphat (PLP), 1-Pyridoxin-5-Phosphat (PNP) und Pyridoxamin-5-Phosphat (PMP) sowie das Endprodukt des Vitamin-B-Metabolismus 4-Pyridoxalsäure. Allgemein anerkannt ist, dass Pyridoxal-5-phosphat der wirksamste Bestandteil ist, wobei für den Vitamineffekt aber auch die Verhältnisse der einzelnen Metabolite entscheidend sind.
Insgesamt empfehlen wir, wenn es um die „Versorgungssituation“ bei Patienten mit chronischen Entzündungen geht, den Bioaktivitätstest zu wählen und sich bei der Substitution hinsichtlich Dosis und Präparateauswahl an den Aktivitätswerten zu orientieren.
Mehr zu diesem Thema finden Sie auf unserer Diagnostikinformation Nr.: 307
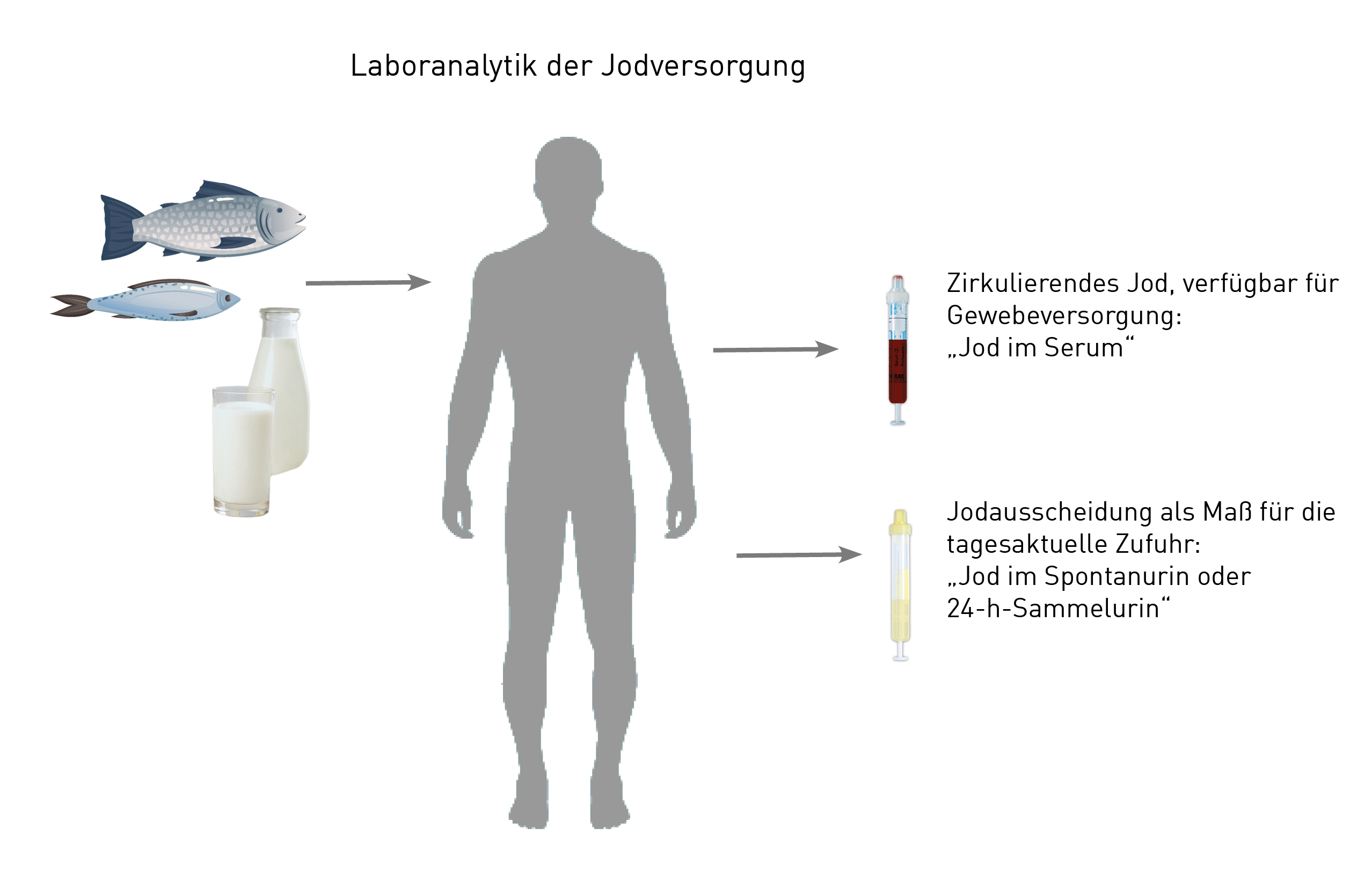
Grundsätzlich ist die Analyse sowohl aus Spontanurin, 24-Stunden-Sammelurin als auch aus Serum und EDTA-Blut gleichermaßen möglich. Es bestehen jedoch Unterschiede in der Aussagekraft zwischen den Materialien:
- Wir empfehlen zur Messung der aktuellen Jodversorgung die Analyse von Spontanurin oder 24-Stunden-Urin. Aufgrund der simplen Probengewinnung wird in der Praxis häufig Spontanurin bevorzugt. Dennoch liefert die Analyse von 24-Stunden-Urin ein exakteres Ergebnis, weil Schwankungen im Tagesverlauf ausgeglichen werden.
- Die Serumanalyse hingegen zeigt die Menge an im Blutkreislauf zirkulierendem Jod an. In den Messwert fließt auch das an Schilddrüsenhormone gebundene Jod ein. Der Serumspiegel wird daher durch Veränderungen des Schilddrüsenstoffwechsels mit beeinflusst. Anders als bei Mineralstoffen bietet die Messung von Jod im EDTA-Vollblut keinen Vorteil gegenüber der Serumanalyse. Im EDTA- wie im Heparin Vollblut sind regelmäßig niedrigere Spiegel zu finden.
Darüber hinaus ist die Jodbestimmung im Rahmen des „Jodsättigungstests nach Dr. Abraham“ möglich. Hier wird die Sättigung von Organen/Gewebe mit Jod untersucht. Nach Gabe einer hohen Dosis
Jod wird die Ausscheidung im 24-Stunden-Urin gemessen. Nach Dr. Abraham ist eine Jodsättigung des Gewebes erreicht, wenn mindestens 90 % der Zufuhr wieder ausgeschieden werden. Die bei diesem Test verabreichte Dosis überschreitet i. d. R. bei weitem die Menge, die schulmedizinisch als sichere Tagesdosis angesehen wird. Ob der Jodsättigungstest bei einem Patienten durchgeführt werden soll, erfordert daher eine sorgfältige klinische Evaluation durch den behandelnden Arzt.
Die am häufigsten angewandte Methode für den Nachweis des Vitaminenspiegels ist die Mengenbestimmung mittels chromatographischer Analyseverfahren (u. a. HPLC). Dieses kann im Serum, EDTA-Plasma oder auch intrazellulär erfolgen (im Blutkuchen nach Abtrennung flüssiger Blutbestandteile). Dieses quantitative Verfahren differenziert jedoch nicht zwischen aktiven und inaktiven Vitaminmetaboliten. Die Blutproben für die Bestimmung der Vitaminaktivität (ID-Vit®) werden enzymatisch vorbehandelt und verdünnt in eine Mikrotiterplatte gegeben, die je nach Vitamin mit vitaminsensitiven Lactobacillus fermentum, Lactobacillus rhamnosus bzw. Saccharomyces cerevisiae beschichtet sind. Das für jedes Vitamin individuell zusammengesetzte Medium enthält alle für ein Bakterien-/ Hefewachstum notwendigen Bestandteile mit Ausnahme des jeweils zu messenden Vitamins. Nach Zugabe des Patientenblutes wächst die Bakterienkultur, bis das (aktive) Vitamin aufgebraucht ist. Das Wachstum der Bakterien wird nach 72 h als Trübung im Photometer gemessen und mit einer Standard-Konzentrationsreihe verglichen. Die Menge an bioaktivem Vitamin im zugegebenen Patientenblut ist dabei direkt proportional zum Bakterien-/ Hefewachstum.

FAQ Kategorien
